鋰在大腦中發揮神祕作用,能否用以防範阿爾茲海默病?

地球是一個奇蹟
文化|全球
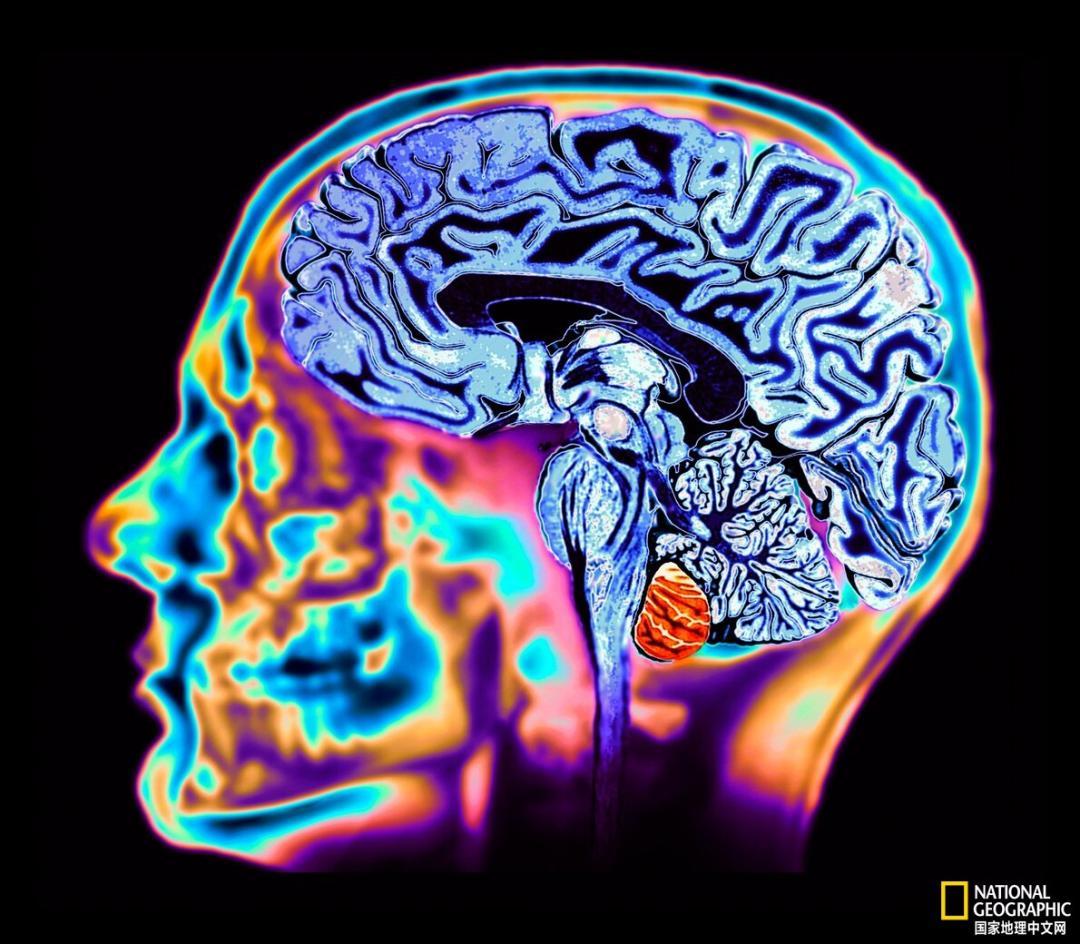
長期以來,鋰療法一直是雙相情感障礙的基礎治療方案。越來越多證據表明,缺鋰可能是阿爾茲海默病的一個致病因素。鋰的作用機制尚未解明,而接下來這篇文章將介紹,關於這種銀白色輕金屬如何影響大腦,我們都知道些什麼。|合成攝影:ZEPHYR/SCIENCE PHOTO LIBRARY

有一些元素已知爲生命之必需:碳、氧、氫、氮和磷。還有一些關鍵次要元素:鐵、鈣、鉀和鈉。過去很長時間,鋰似乎一直被歸爲第三類元素(就像鈦或鐳)——除非身體有恙,否則不得入體。
鋰爲電池等人類發明的諸多技術供能,同時還作爲一種有效的治療手段,常年出現在醫生針對雙相情感障礙和部分重度抑鬱開具的處方上。然而“直到不久前,我們纔開始考慮鋰在生理層面的必要意義。”加拿大達爾豪斯大學精神病學專家托馬斯·哈耶克(Tomas Hajek)說。
如今,研究正在表明,低劑量鋰有可能阻斷甚至扭轉阿爾茲海默病和認知衰退的侵襲。科學家仍在努力瞭解鋰的作用機制,他們逐漸認識到,這種金屬元素或將加入人體(尤其是大腦)生存必需的元素清單。
投入運用
自從鋰在1817年被發現以後,科學家就開始研究這種銀白色輕金屬,用它治療“一般焦慮症”等精神疾病。20世紀初,鋰產品真正開始湧現。七喜汽水(7-Up)的一套早期配方就含有鋰,這也是飲料名稱的一種來由(另一個解釋是,七喜汽水最初有七種成分)。“名稱中的‘up’大概指向鋰改善心理狀態的功效,‘7’則代表其分子量。”哈佛醫學院神經科學家布魯斯·楊克納(Bruce Yankner)說。與那個時代許多專利藥物和補品一樣,產品所含的鋰劑量大、有毒性。如今七喜已剔除了這項分子量爲7的“振奮劑”。
鋰消費歷經一段低迷後,1949年,澳大利亞醫生約翰·卡德(John Cade)成功開始用鋰治療雙相情感障礙;1970年,鋰劑在美國通過批准。“可以說,鋰成了情緒穩定治療的金標準。”哈耶克解釋說。
沒人特別清楚鋰如何減輕躁狂、緩解抑鬱。不過,這是次要問題,鋰首先確能挽救生命。“聽上去有一定爭議性,”哈耶克說,“但不需要我理解原理,事物也會自發運轉……要是我們一開始就想摸清運轉規律,則恐怕根本不會找到任何精神病藥方。”
雙相障礙的患者服用碳酸鋰形式鋰劑,鋰含量極高;服藥患者需受密切監視,以確保藥物不會給腎臟、甲狀腺等更多部位帶來副作用。
潛在腦功效
鋰可能具有神經保護功效的第一個線索,就來自雙相患者。智利聖地亞哥大學精神病學專家保羅·弗林格(Paul Vöhringer)解釋說,隨着年齡增長,嚴重情緒障礙者出現認知損傷的風險是常規水平的三倍。然而2007年,瑞士科學家證實,採用鋰治療的雙相患者“罹患認知症或阿爾茲海默病的幾率與一般人羣趨同,與未採取鋰治療的患者對比鮮明。”鋰療法似乎讓患者原先增大的風險落回人羣水準。
其後,在2012年,哈耶克掃描患者大腦,發現了海馬體的差異——這是有關記憶力的重要腦區,對於重度抑鬱和雙向情感障礙也很關鍵。“重度抑鬱人羣的海馬體通常更小。”他講解道。但接受鋰治療的患者,其海馬體體積看起來很正常。“他們的大腦基本完好無缺,儘管實際上病史很長。”哈耶克說。
即便是極少量的鋰(見於人口飲用水等),也被證明與攻擊性、自殺率及認知衰退的羣體水平降低有關。“這實在是謎團重重,按說人們從飲用水中攝取的鋰劑量與我們臨牀使用的劑量相差好幾個數量級。”哈耶克說。
與阿爾茲海默病的聯繫
恰巧,楊克納實驗室曾在阿爾茲海默病研究中用鋰測試單一wnt信號通路可以激活哪些神經保護因素。“使用高濃度鋰是實驗室激活wnt的經典做法。”他說。在動物模型當中,“這種高濃度鋰不說百分之百,也足以扭轉大量(阿爾茲海默病)病理表現。”研究人員開始猜測:“鋰本身是否有可能是致病機理的構成部分?”
揚克納與同事從考察屍體大腦開始,他們發現,正常大腦只含有基礎水平的鋰,因爲含量太低,沒被此前研究檢測出來。認知正常人羣的神經組織含有微量鋰,“幾乎是接受高劑量鋰治療的雙相患者的千分之一。”他說。而生前有輕度認知障礙或阿爾茲海默病的死者,其大腦中的鋰含量還要更加微不可見。
這些鋰會到哪裏去?楊克納與實驗室成員成功發現,鋰緊緊依附“一團團β-澱粉樣蛋白斑塊”——具體說來是由42個氨基酸構成的蛋白,它關係着阿爾茲海默病的發展,他解釋說。這些斑塊可能吸收了大腦儲存的鋰。
“我們從食物和水源中攝入鋰。”楊克納闡述道。因此,爲了弄清鋰離子的真正角色,實驗室剝奪了小鼠從飲食中正常攝入的92%的鋰。雖然該舉措讓小鼠血液中的鋰水平下降了90%,但楊克納指出,大腦中的鋰只減少了50%——意味着大腦還在保證鋰供給。“顯而易見,大腦內有一個鋰資源池。”
在阿爾茲海默病小鼠模型中,下降50%亦有深遠影響。澱粉樣斑塊迅速膨脹,另一種涉及阿爾茲海默病的蛋白——tao蛋白也出現了同樣變化。另外,團隊今年年初在《自然》期刊上報道稱,患鼠的記憶力表現很糟糕,這都是早期認知衰退的跡象。
清除細胞垃圾
鋰是一種小到不可思議的原子,電化學屬性十分活躍,因此很難一語道破到底是它在大腦中的哪一種作用影響着阿爾茲海默。
一種可能的解釋:鋰可以降低糖原合成酶激酶-3β(glycogen synthase kinase-3 beta,簡稱GSK-3β)的活性。後者作爲一種繁忙的分子,牽涉到多種活動,包括調節wnt信號通道(與保護大腦有關)。它也引起了楊克納對鋰的興趣。GSK-3β也作用於tau蛋白,它會吸附額外的磷,造成阿爾茲海默病期間細胞內tau蛋白纏結。抑制GSK-3β還可能激活自噬,讓細胞分解掉不再正常工作的部分,意大利比薩大學和地中海神經學研究所的神經科學家弗朗西斯科·福爾奈(Francesco Fornai)說。
福爾奈提到,阿爾茲海默病患者的細胞自噬是受到抑制的,這就導致β-澱粉樣蛋白斑塊和tau蛋白纖維纏結等細胞“垃圾”堆積。重新激活自噬,細胞就能重啓衛生系統,“這也將帶來認知功能改善。”而鋰元素,他指出,就有激活自噬的能力。
楊克納與實驗室團隊就進行了這麼一項實驗:使用乳清酸鋰這種低劑量鋰劑,恢復實驗體鋰水平。β-澱粉樣蛋白斑塊和tau蛋白的堆積終止了。小鼠重拾記憶功能。研究者們僅使用了遠低於當前雙相患者鋰療法的劑量,就實現了這一切。
一項臨牀要素
小鼠模型結果喜人,不過暫時還沒人把鋰加回碳酸飲料裏去。下一步是進行臨牀試驗,判斷何種形式和劑量的鋰劑能安全、有效地治療人類認知衰退問題。
弗林格目前正在智利招募臨牀志願者,尋找有情緒障礙的老年患者——這個羣體有較高的風險出現認知損傷。弗林格希望能爲部分受試者進行長達五年的低劑量鋰治療,劑量定在50mg左右(雙相情感障礙患者的劑量通常爲300mg起步),由此檢驗鋰治療能否防患輕度認知障礙。
可資金問題向來較難克服,弗林格說。“沒人用鋰掙錢,因爲它基本上是種天然產物,”他說,“好比用氧氣或水來掙錢一樣;它不是藥物。”這就導致鋰價格低廉,但也沒什麼利益空間,大型藥企沒有多少動力操辦測試。楊克納還計劃使用乳清酸鋰完成更多研究。
關於這種微小元素的作用,尚有諸多疑問。“我們還未徹底摸清鋰在大腦中的生理意義。”楊克納說,這可能涉及β-澱粉樣蛋白、tao蛋白和GSK-3β。“不過還有一種可能,我不會排除:那就是鋰可以直接影響大腦電化學機制,恰如它在鋰電池中的作用,”他說,“可能我們本非這一獨特電化學性質的首個發現者和使用者,也許生物演化比我們更早找到它。”
深入研究是獲取知識的關鍵,但對於弗林格等精神病學專家,臨牀實踐需要先行。“我不會坐等前景清晰纔去治病,”他說,“假如我們做鋰治療能讓患者情況好轉,那就放手去做。”
撰文:Bethany Brookshire
編譯:綠酒
校對:錢思琦
版式設計:錢思琦

點點,謝謝關注。
伸出小手


















