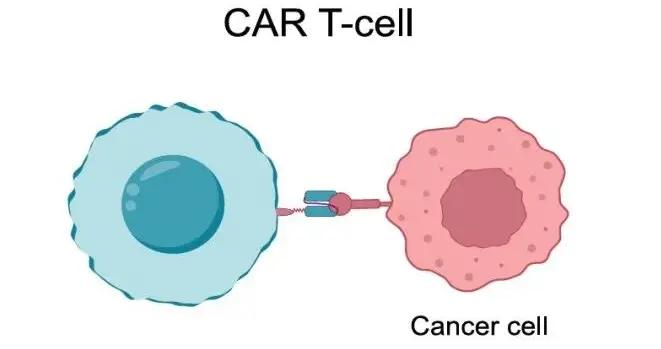
細胞接觸時可能互"咬"一口,科學家:這不就是天然快遞嗎?
在美國斯坦福大學生物工程系亓磊副教授的實驗室裏,博士生陳心怡盯着顯微鏡的屏幕,感到十分困惑。
她原本想讓嵌合抗原受體T(CAR-T)細胞識別並殺死癌細胞,可詭異的是,一些CAR-T細胞的表面竟然出現了不屬於它們的分子,這些分子似乎是從癌細胞身上“偷”來的。
陳心怡的導師亓磊多年來一直關注着免疫細胞之間的相互作用。瞭解到這件事後,亓磊告訴陳心怡,這或許正是“胞啃”(trogocytosis)現象。
去抓犯人的臥底警察,同伴卻以爲你已經叛變
所謂“胞啃”,描述的是一種奇特的細胞行爲:當兩個細胞緊密接觸時,它們會從對方細胞表面“啃”下一小塊細胞膜,連同膜上的分子一起轉移到自己身上。這是一個古老的機制,早在20世紀70年代,免疫學家就注意到了這種奇特的現象。但直到21世紀初,它纔有了“胞啃”這個形象而略顯粗暴的名字。
這個看似簡單的過程,既是陳心怡所面臨的難題,多年來也一直困擾着免疫學家:當CAR-T細胞緊貼癌細胞併發生胞啃後,它們可能會把癌細胞表面的一些標誌性分子帶到自己身上。於是,這些原本負責追殺癌細胞的免疫細胞,外表就會開始變得像癌細胞。
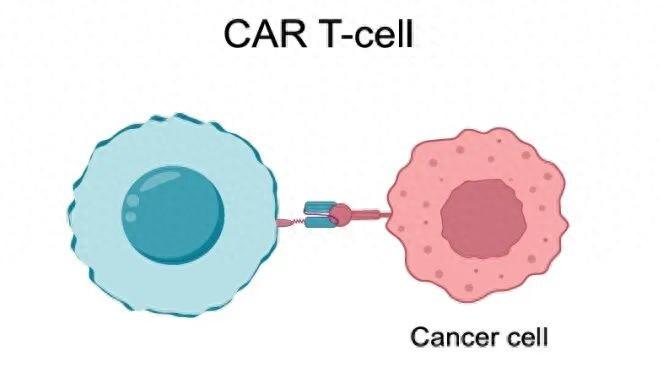
CAR-T細胞原本應精確識別並殺死癌細胞丨圖蟲創意
這會帶來雙重麻煩。一方面,這些被“污染”的CAR-T細胞自身功能有可能受損。同時,其他CAR-T細胞又可能將變了樣的同伴錯當成癌細胞,轉而攻擊隊友。
亓磊打了個比方,用電影《無間道》來形容這種困境:你本來是去抓犯人的臥底警察,結果同伴卻以爲你已經叛變,反過來要置你於死地。
翻閱着一篇又一篇關於“胞啃”的論文,陳心怡心裏有些沮喪,原來這並不是什麼新鮮發現。幾十年來,科學家一直在試圖阻止胞啃的發生,把它當作必須消除的副作用。但亓磊和陳心怡意識到,胞啃不只是副作用,而是一個大自然已經優化了幾億年的“接口”。
兩個細胞只要“握一下手”,就能將自己表面的分子帶到對方身上。這難道不是一種天然的遞送機制嗎?只不過與傳統的遞送方式不同,這裏負責運貨的是一個活生生的細胞。這種特殊之處或許正是解決藥物遞送難題的關鍵,尤其是CRISPR等基因編輯工具的遞送。
基因編輯的三大挑戰:遞送、遞送、遞送
對亓磊而言,這正是他夢寐以求的目標。從博士階段開始,他就在研究和開發基於CRISPR的基因編輯工具。2012年,他曾與其博士生導師、身爲諾獎得主的CRISPR技術先驅珍妮弗·杜德納(Jennifer Doudna)合作,是最早一批探索利用CRISPR進行基因編輯的研究者之一。
再強大的基因編輯工具,也都得先送進細胞才能發揮作用,但在活體內直接使用CRISPR進行基因編輯始終困難重重。CRISPR技術誕生至今已有十幾年,但真正能在臨牀體內應用的目前也只有一兩個。許多正在臨牀測試中的療法,效果也不及預期。
問題並不出在CRISPR技術本身,而是卡在了遞送上。

CRISPR技術誕生至今已有十幾年,但真正能在臨牀體內應用的目前也只有一兩個丨圖蟲創意
目前能用來遞送基因編輯工具的辦法並不多,主流選擇無非是病毒載體和脂質體等。但病毒遞送伴隨着安全性和免疫原性方面的擔憂,脂質體遞送又容易富集到肝臟,因此針對肝臟以外的疾病往往效果不佳。
遞送難題早已成爲基因編輯領域的共識,甚至是整個生物醫學界都默認的一道難關。諾獎得主、研究生物正交化學的卡羅琳·貝爾託齊(Carolyn Bertozzi)和亓磊的實驗室在斯坦福大學的同一棟樓,她曾半開玩笑地對亓磊說:“你們基因編輯領域最大的三個挑戰,就是遞送、遞送、遞送。”
而胞啃或許就是這個突破口。亓磊認爲,在基因編輯領域,人們過去更多是在現有遞送方式上修修補補,試圖解決其中的問題並提升效果,但這些方法從一開始就帶有某些根本性的限制。他們需要走一條全新的路徑,看看能否解決現有方法無法解決的問題。
生物學家裏,十有八九都沒聽說過它
可真要把胞啃變成一種遞送工具,遠沒有聽上去那麼簡單。
胞啃被發現至今已經過去了幾十年,但科學家對它的瞭解依然相當有限。這個詞在生物學之外幾乎鮮爲人知,就連在專業圈子裏,它也算不上一個廣爲人知的概念。亓磊估計,即便是有生物學背景的人,十個裏恐怕也有八個沒聽說過胞啃。
更麻煩的是,科學家對於胞啃的瞭解,還停留在現象描述上。人們只知道某些細胞類型之間能發生胞啃,卻並不清楚它是如何開始的,以及背後有哪些分子機制。至於那些被“啃”下來的細胞膜和膜上的分子,在進入另一個細胞之後會經歷什麼,也都沒有清晰的答案。
陳心怡手裏並沒有可供參考的“地圖”,卻要在這樣的基礎上開發一種全新的遞送工具,這無疑是一場冒險。不過在亓磊看來,科學研究正需要這種更前瞻、更具探索性的嘗試。他回憶起2012年開始研究CRISPR技術時的情景,那時他連Cas9長什麼樣都不知道,可還是硬生生將它改造成了能在細胞裏調控轉錄的CRISPRi工具。
正是抱着這樣的探索心態,他們決定一邊研究胞啃的機制,一邊試着將它改造成一種用於遞送的工具。
研究很快有了一些發現。胞啃現象發生需要滿足一定條件,它取決於胞啃細胞表面是否存在特定的分子“指紋”,能否相互識別並進而“握手”。只有當兩個細胞建立起足夠“親密”的連結,胞啃纔會發生。同時胞啃現象發生得非常快,兩個細胞接觸之後,往往幾分鐘內就會開始相互“啃食”。
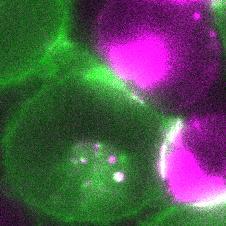
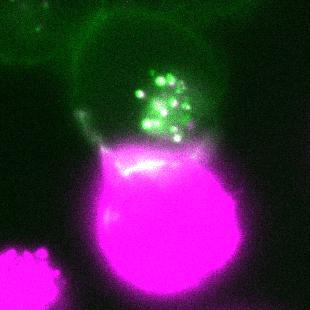
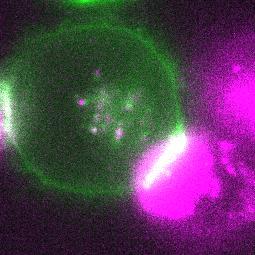
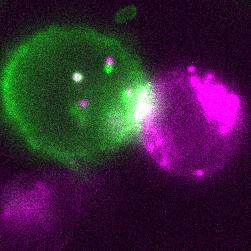
粉色細胞正在通過胞啃將紅色熒光蛋白mCherry遞送給綠色細胞丨受訪者供圖
而且,能夠發生胞啃的細胞可能遠比人們以爲的多得多。他們在實驗室裏測試了近10種細胞,結果都能發生胞啃。結合人類蛋白質圖譜(Human Protein Atlas)數據庫進一步推算,他們發現人體內很可能有近100種細胞都能通過特定方式被精準引導發生胞啃。
一個思路逐漸清晰起來:既然CAR-T細胞療法的核心是改造T細胞,讓它特異而緊密地結合癌細胞,那麼同樣的方法也許可以被化用到這裏。只要讓改造後的細胞能主動、精準地貼近目標細胞,那麼它或許就能借助胞啃,把自己攜帶的成分遞送出去。
向自然學習,或可絕處逢生
但事情再次偏離了設想。
當陳心怡開始嘗試用工程化改造過的細胞來遞送時,她發現儘管這些細胞能將細胞膜上的分子遞送給目標細胞,但絕大部分遞送過去的分子都沒有功能。它們進入了目標細胞的溶酶體,被那裏的酸性環境降解了。她嘗試了不少辦法,結果都是如此。
陳心怡不得不重新審視前人的觀察。過去一些研究曾報道某些分子會通過胞啃出現在其他細胞表面,但現在看來,這些分子未必真的具有功能。它們有可能只是粘在那兒,很不穩定,洗幾次就掉了。
這個發現一度讓她非常沮喪。前人的研究經驗可能並未展現故事的全貌,她不能把那些結論視爲理所當然。
不過,既然能從“糟糕”的胞啃現象中找到新用途,那麼能否也從溶酶體出發尋找突破口,讓那些分子在降解之前逃離溶酶體呢?順着這個思路,他們開始嘗試前人用過的一些策略,仍然一次又一次地失敗了。
接連碰壁之後,他們選擇將目光重新投回自然界本身。多年來,亓磊實驗室一直秉承着一個原則:很多看似棘手的技術難題,也許早已在自然演化中出現了某種解法。從大自然中尋找靈感,把自然界中的東西變成人類能夠利用的東西,也是研究生物工程的樂趣所在。
於是他們提出了一個思路:向病毒學習。自然界中的某些病毒在感染細胞後,必須先進入較早期的溶酶體,再設法逃逸出來,才能繼續生命歷程。如果病毒能在這樣的環境中成功脫身,那麼病毒身上的某些元件也許能幫助那些通過胞啃進入細胞的分子逃離溶酶體。
最終,他們找到了水皰性口炎病毒上的一種蛋白質——VSVG。陳心怡試着把VSVG整合到了用於胞啃遞送的工程細胞表面。這次的結果終於不一樣了:目標細胞表面明顯出現了由工程細胞遞送而來的、有功能的蛋白質。更讓人興奮的是,這一現象在他們測試的幾乎所有目標細胞類型中都能看到。
胞啃遞送示意圖丨ChatGPT
沿着酸性環境這條線索,他們又找到了一段會在酸性條件下自動切割的氨基酸序列,並把它接到了想遞送的目標蛋白質上。這樣一來,當這些蛋白質隨着胞啃進入目標細胞內部、到達早期溶酶體後,就會在酸性環境中從膜上脫落,再借助VSVG逃離至目標細胞的細胞質乃至細胞核。陳心怡把這個過程形容爲“坐纜車”:遞送的蛋白質先借由胞啃進入目標細胞,然後在溶酶體裏下車,最終去往自己真正該去的地方。
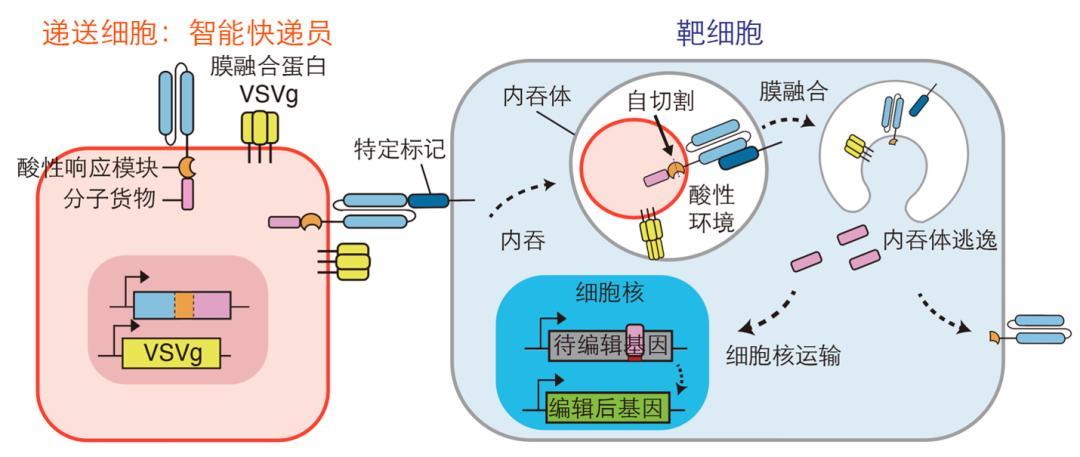
胞啃遞送機制丨受訪者供圖
由此,通過胞啃遞送的蛋白質類型和用途也大大拓寬了。藉助這些“胞啃使者”,他們不僅遞送了基因編輯工具,也遞送了能用於殺傷癌細胞的成分,甚至還遞送了鹼基編輯器這類體積更大、通常難以用病毒等方法運送的分子機器。
最終,他們將這些結果整理成論文,並於今年4月發表在了《自然·細胞生物學》[1](Nature Cell Biology)上。
去思考一些邊緣、甚至奇怪的問題
不過在亓磊看來,這些成果只是一個開始。
成功讓活細胞利用胞啃來遞送大分子固然是關鍵的一步,但亓磊還有更大的野心,他希望將這些“胞啃使者”開發成可編程的活體遞送系統:當這些細胞進入體內後,它們將能自主識別多種疾病信號,主動抵達該去的器官和靶細胞。
亓磊認爲,這種設想背後也許是一種新的醫學圖景:“傳統藥物都是基於化學的,但未來的醫學將很大程度上基於生物學。基於活細胞來製藥是我們的願景。這種方法能實現傳統化學藥物無法實現的精準性和可編程性。”從發明CRISPRi來調控基因轉錄,到利用胞啃來解決遞送問題,他的研究始終是構建一套完整的生命編程系統。
爲了走向這個目標,他們還要回答許多更具體的問題。比如,不同類型細胞之間的胞啃究竟有哪些差異,哪種細胞更適合在體內充當“胞啃使者”,以及一旦這種方法真的在人體內應用會造成哪些影響。
在免疫治療中,胞啃常常以副作用的面貌出現。可在正常生理條件下,胞啃究竟扮演着什麼角色,人們並不完全清楚。它或許是細胞之間交換信息的一種方式,或許能增強某些細胞的功能,也可能參與免疫系統的調節。但這些猜想大多還在等待更加紮實的證據。

亓磊(左)和陳心怡(右)丨受訪者供圖
對陳心怡而言,這條路走到現在,最深的感受是科研的不確定性。她說:“科研沒有一條最好的路徑,也很難有什麼時間點來判斷自己做的東西究竟還能走多遠。我們總是在遇見預期之外的事情,有時是驚喜,有時是失敗,但這也正是科研最美妙的點。”
而在亓磊看來,他們的工作提醒着人們,奇怪的現象背後通常隱藏着更重要的生物學意義,它們值得深入研究。他說:“我們不是在修補一個現有的工具,而是在定義一種全新的遞送範式。通過胞啃,我們讓細胞具備了像生物計算機一樣精準傳輸信息的能力。這正是編程生命的核心。”
參考文獻
[1] https://www.nature.com/articles/s41556-026-01920-0
作者:黃雨佳
編輯:黎小球
封面圖來源:Nano Banana 2

本文來自果殼,未經授權不得轉載.
如有需要請聯繫[email protected]
點個“小愛心”吧