牙沒刷好,竟然會助推癌細胞轉移?看完立馬想去刷牙!
誰能想到,牙沒刷好,竟然會促進癌細胞轉移?
2025 年 12 月,武漢大學的研究團隊發表了一項引人關注的研究。他們發現,一種常見的牙周致病菌——牙齦卟啉單胞菌——可能會通過釋放微小的“囊泡”,影響食管鱗狀細胞癌的轉移過程[1]。
簡單來說,這項研究揭示了一條可能的生物學機制:來自口腔的細菌產物,或許能夠通過一系列細胞內信號變化,推動癌細胞更容易擴散。
但在焦慮之前,有必要先把事實放回科學語境中,看清這些研究到底告訴了我們什麼,又沒有告訴我們什麼。
從“口腔細菌”到“腫瘤轉移”,
證據不斷積累
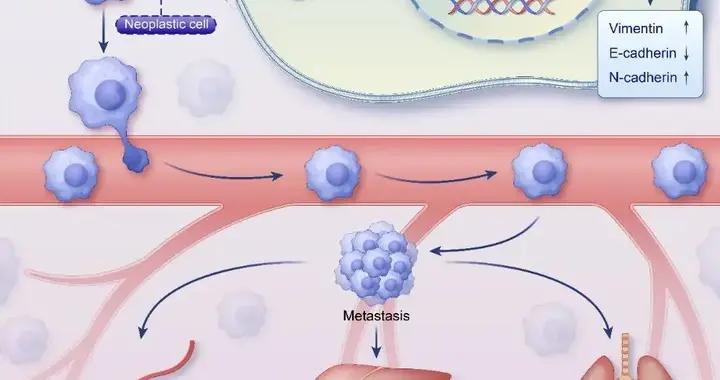
武漢大學的這項研究首先在食管鱗癌組織中發現,牙齦卟啉單胞菌在腫瘤組織中的丰度明顯高於鄰近正常組織,並且其丰度越高,患者的分期越晚、淋巴結轉移越多、生存時間也越短[1]。進一步的細胞和動物實驗顯示,這種細菌釋放的細胞外囊泡可以增強腫瘤細胞的遷移和侵襲能力,從而推動轉移發生。
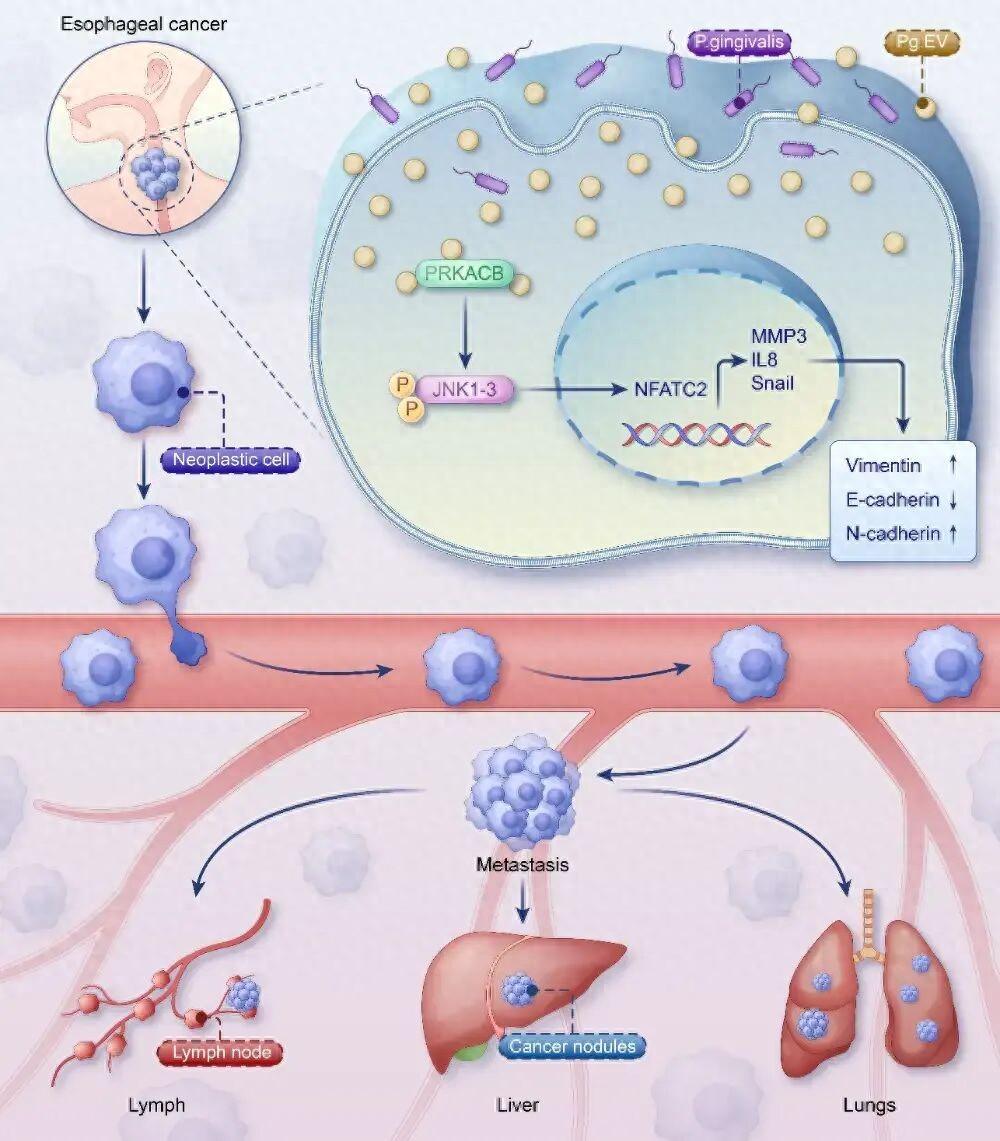
牙齦卟啉單胞菌胞外囊泡促進食管鱗癌進展的機制示意圖 | 參考資料[1]
這並不是孤立的發現。另一項基於轉錄組數據的研究顯示,牙齦卟啉單胞菌感染可顯著改變食管鱗癌細胞的炎症相關基因表達特徵,感染相關基因特徵明顯的患者,整體生存時間更短[2]。
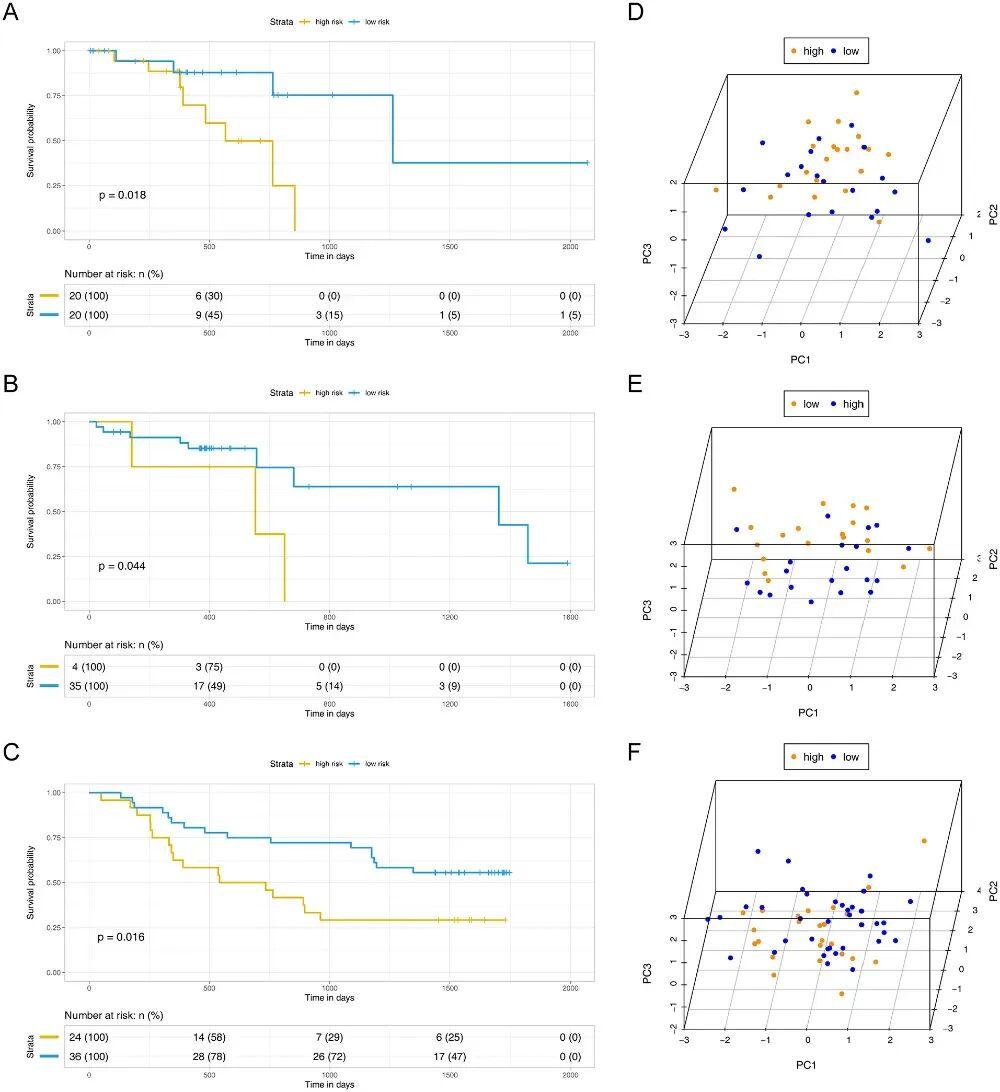
(A–C)根據“牙齦卟啉單胞菌感染相關基因特徵”的表達水平,研究人員將患者分爲高表達組和低表達組,比較兩組患者的總生存期(Kaplan–Meier 生存曲線) | 參考資料[2]
這些研究從分子層面支持了一個觀點:慢性的口腔感染,可能通過炎症和信號通路重塑腫瘤微環境,從而影響疾病進展。
流行病學研究同樣支持了這個結論。
一項回顧性研究比較了 60 例食管鱗癌患者與 178 名健康對照者,發現牙周附着喪失更重、缺牙更多的人羣,在食管鱗癌患者中所佔比例更高[3]。而在接受食管癌根治手術的患者中,術前合併中重度牙周炎者,其長期生存狀況明顯差於牙周狀況良好的患者[4]。
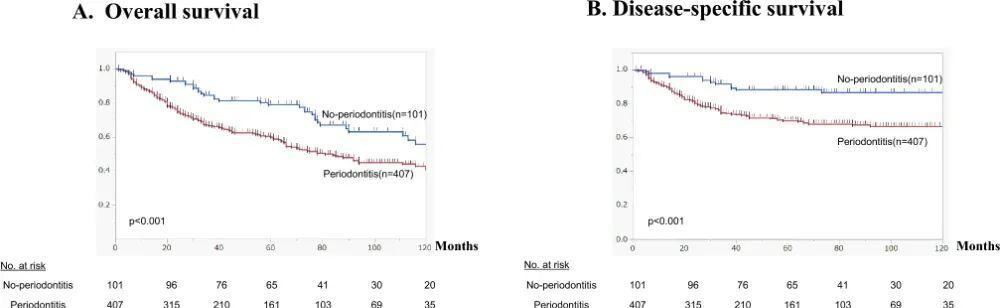
食管切除術後患者牙周炎(伴或不伴牙周炎)與總生存期(OS)(A)和疾病特異性生存期(DSS)(B)之間的關聯 | 參考資料[4]
類似的關聯在其他地區和其他消化道腫瘤中也被觀察到。克什米爾地區的一項大型病例對照研究顯示,與從不清潔牙齒的人相比,至少偶爾清潔牙齒的人羣中,食管鱗癌患者所佔比例明顯更低[5]。而在中國西南地區的嵌套病例對照研究中,牙周炎人羣中食管癌、結直腸癌的比例約爲無牙周炎人羣的兩倍左右,同時在部分腫瘤類型中,還與轉移發生更爲常見相關[6]。
相關不等於因果:
我們應怎樣理解這些發現?
看到這些結果,很多人會下意識地問:是不是有牙周病,就一定會得消化道腫瘤?答案是否定的。
現有研究大多提示的是相關性,而不是確定的因果關係。牙周疾病往往與吸菸、飲酒、飲食結構、社會經濟狀況等因素同時存在,這些因素本身就是消化道腫瘤的重要影響因素。即便在統計分析中進行了調整,也無法完全剝離所有混雜因素的影響。
與從不清潔牙齒的人相比,至少偶爾清潔牙齒的人羣中,食管鱗癌患者所佔比例明顯更低
此外,從機制研究到真實世界,還隔着很長一段距離。武漢大學的研究爲我們提供了一個清晰的分子解釋框架,但這並不意味着在普通人羣中,牙齦卟啉單胞菌就一定會通過同樣的路徑推動腫瘤發生。更多情況下,它可能只是參與了一個長期炎症網絡,而不是單一開關。
因此,更合理的理解是:牙周疾病可能是消化道腫瘤發生和進展的一個伴隨風險因素,而不是決定命運的因素。
不製造恐慌,但也不忽視:
普通人能做什麼?
這些研究是在提醒我們,口腔健康和身體其他器官息息相關,長期存在的炎症狀態,確實可能通過多種方式影響全身健康。
對大多數人來說,這並不意味着要頻繁篩查腫瘤,更不意味着一發現牙周問題就聯想到癌症。真正有意義的,是把口腔健康納入日常健康管理的一部分。
規律刷牙、使用牙線、減少長期牙齦出血和牙周感染的狀態,本身就能改善生活質量,也可能在長期內降低慢性炎症負擔。

真正有意義的,是把口腔健康納入日常健康管理的一部分
對於已經被診斷爲消化道腫瘤的患者,這些研究則提供了一個值得重視的臨牀細節。多項研究顯示,術前或治療前進行規範的口腔評估和處理,與更好的預後相關[4]。但這並不是“治牙就能治癌”,而是減少感染和炎症負擔,讓身體在治療過程中處於更有利的狀態。
科學的價值在於幫助我們做出更理性的選擇。牙周疾病與消化道腫瘤之間的聯繫,正在被一點點勾勒清楚,而我們能做的,仍然是那些最基礎、也最穩妥的事情——把每天的口腔清潔,當作對身體的一種長期投資。
參考文獻
[1]Hong K, Zhang H, Qi J, et al. Porphyromonas gingivalis extracellular vesicles promote tumor metastasis in esophageal squamous cell carcinoma by inducing the PRKACB/JNK/NFATC2 axis. J Nanobiotechnology. 2026;24:66.
[2]Kong J, Liu Y, Wang J, et al. A novel Porphyromonas gingivalis infection-related inflammatory response gene signature predicts the prognosis of esophageal squamous cell carcinoma. Clin Med Insights Oncol. 2024;18:1–15.
[3]Haque T, Nabhan AB, Akhter F, et al. The analysis of periodontal diseases and squamous cell esophageal cancer: a retrospective study. Saudi Dent J. 2023;35:714–719.
[4]Nozaki S, Sato Y, Takano H, et al. Pretreatment periodontitis is predictive of a poorer prognosis after esophagectomy for esophageal cancer. Esophagus. 2024;21:120–130.
[5]Dar NA, Islami F, Bhat GA, et al. Poor oral hygiene and risk of esophageal squamous cell carcinoma in Kashmir. Br J Cancer. 2013;109:1367–1372.
[6]Luo T, Li J, Pu K, Yang G. Association between periodontitis and gastrointestinal cancer risk and prognosis: evidence from a nested case–control study in Southwest China. Eur J Med Res. 2025;30:225.
策劃製作
作者丨蔣永源 第三軍醫大學內科碩士
審覈丨潘戰和 廈門大學附屬中山醫院腫瘤內科主任醫師 福建省抗癌協會腫瘤科普專業委員會副主任委員
策劃丨何雨濛
責編丨何雨濛
審校丨徐來、張林林