全球新!來自上海!首款侵入式腦機接口醫療器械獲批上市


記者今日從上海藥監最新獲悉:近日,國家藥監局批准了博睿康醫療科技(上海)有限公司植入式腦機接口手部運動功能代償系統創新產品註冊申請,實現腦機接口醫療器械全球首發上市,標誌着國際首個侵入式腦機接口醫療器械進入臨牀應用階段。
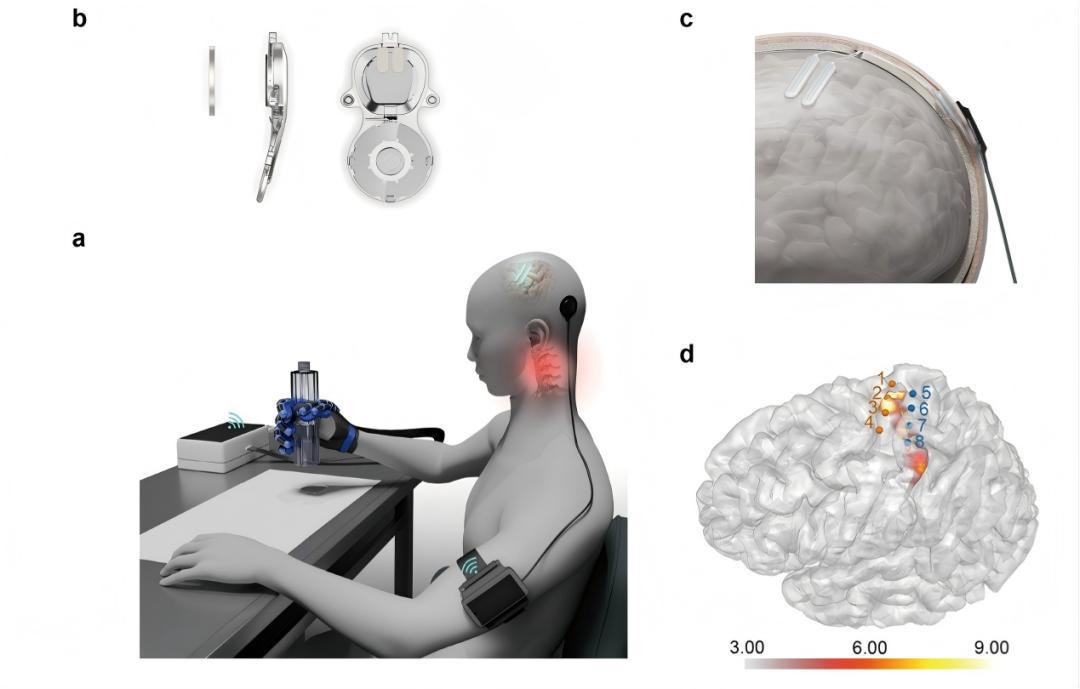
該產品由腦機接口植入體、植入式腦電電極套件、腦電信號收發器、氣動手套設備、一次性手術工具包、腦電解碼軟件、醫用測試軟件、臨牀管理軟件組成。適用於頸段脊髓損傷所致四肢癱患者,通過氣動手套設備輔助實現手部的抓握功能代償。患者需滿足以下條件:18歲到60歲,C2~C6頸段脊髓損傷評級A~C級的四肢癱,疾病確診超過1年且經規範治療後病情穩定至少6個月,手部無法完成抓握,上臂尚存部分功能。該產品採用硬腦膜外微創植入與無線供能通信技術,臨牀試驗結果顯示,受試者通過該產品實現了手部抓握能力的明顯提高,進而改善患者生活質量。

近年來,國家藥監局堅決貫徹落實黨中央、國務院關於健全支持創新醫療器械發展機制重大決策部署,出臺細化舉措,強化部門協同,鼓勵醫工融合和科研轉化,全力支持高端醫療器械重大創新,促進更多新技術、新材料、新工藝和新方法應用於醫療健康領域。腦機接口作爲“十五五”規劃綱要確定的未來產業,國家藥監局高度重視,在產品審評審批中傾斜資源,按照“提前介入、一企一策、全程指導、研審聯動”原則,對創新產品開展前置審評服務,有效加快產品上市進程,切實提升了我國高端醫療器械國際競爭力。
下一步,國家藥監局將繼續做好高端醫療器械審評審批工作,切實以高效能監管助力醫療器械產業高質量發展,造福人民羣衆高品質生活。本市藥品監督管理部門將加強該產品上市後監管,保護患者用械安全。
相關推薦