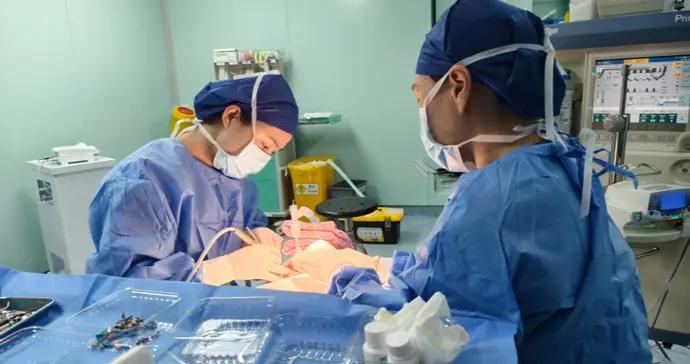
上海科學家臨牀治癒1型糖尿病!吊水30分鐘,擺脫胰島素




圖爲研究團隊合影,前排左一爲殷浩,前排右一爲程新。
上海科研團隊在糖尿病治療領域實現重大突破,在全球首次利用內胚層幹細胞在體外形成再生胰島,通過微創移植,使1型糖尿病患者徹底擺脫胰島素。此舉標誌着糖尿病研究正從過去靠藥物“控制”邁向“功能性治癒”,一個“再生胰島移植治療”的全新時代已然開啓。
該研究由海軍軍醫大學第二附屬醫院(上海長征醫院)殷浩教授團隊聯合中國科學院分子細胞科學卓越創新中心程新教授團隊開展,相關成果近日在國際學術期刊《柳葉刀·糖尿病與內分泌學》發表。
這一重大突破意味着我國在該領域從“跟跑”走向“領跑”。基於相關自主知識產權開發的製劑,已獲中美兩國新藥臨牀試驗(IND)批文,臨牀試驗正嚴謹有序開展,進展順利。未來,隨着技術進一步迭代,糖尿病有望實現全面治癒。
這項重大突破的誕生,除了團隊的努力,也與上海這座城市的科學傳承與創新土壤息息相關。據市科委介紹,在細胞和基因治療(CGT)領域,上海聚焦張江細胞與基因產業園、浦江基因未來谷,已集聚超過200家前沿技術企業,佔國內上下游產業鏈的三分之一。“十四五”以來,上海已有5款CGT產品獲批上市,150多個在研項目進入臨牀階段,多項關鍵指標位居全國前列。

《柳葉刀·糖尿病與內分泌學》近日刊發了相關研究。
中國原創,更安全更高效
我國擁有數百萬1型糖尿病患者,由於其自身胰島細胞被機體免疫系統異常攻擊,導致功能衰竭,血糖難以控制,不得不終身依賴胰島素。雖然傳統胰島移植方法對他們有效,但因爲供體嚴重匱乏(本世紀以來,全球完成的此類移植不過數千例),對廣大患者而言無異杯水車薪。
由此,全球醫學界都在關注一個前沿方向:能否藉助新技術,實現胰島組織的體外規模化再生?上海科研團隊此次給出了極具原創性的中國方案。
要在體外大規模“造胰島”,離不開幹細胞這種“原材料”。此前國際上的通常方案,是以多能幹細胞爲源頭。雖然這種幹細胞可塑性最強,可通過科學的手段,誘導其發育爲包括胰島在內的各種功能性細胞或組織器官,但也因其“多能”,在漫長而複雜的分化過程中,容易混入其他非目標細胞,帶來安全隱患。
殷浩和程新團隊獨闢蹊徑,拋開多能幹細胞,轉而圍繞內胚層幹細胞建立了一套全球獨創的再生胰島技術體系。內胚層幹細胞雖然技術挑戰極大,但優勢明顯:一是分化“潛能”明確,只能形成胰島和肝臟組織;二是分化步驟精簡,可將多能幹細胞的10步壓縮到2步,生產時間從40天左右縮短到14天;最重要的是,這種幹細胞在體內不會無限增殖,可從根本上化解幹細胞治療的成瘤風險。
程新告訴記者,內胚層幹細胞可利用自體或者異體血液細胞製備。其中,自體制備相當於爲每個患者度身定製,耗時長,成本高;異體制備只需選出一位健康人,採集5毫升血液,就能在理論上構建出一個足夠上千萬人使用的內胚層幹細胞“種子庫”。
但問題隨之而來:異體“種子庫”再生的胰島組織,是否會面臨更強的免疫抑制?此次研究也初步找到了答案。
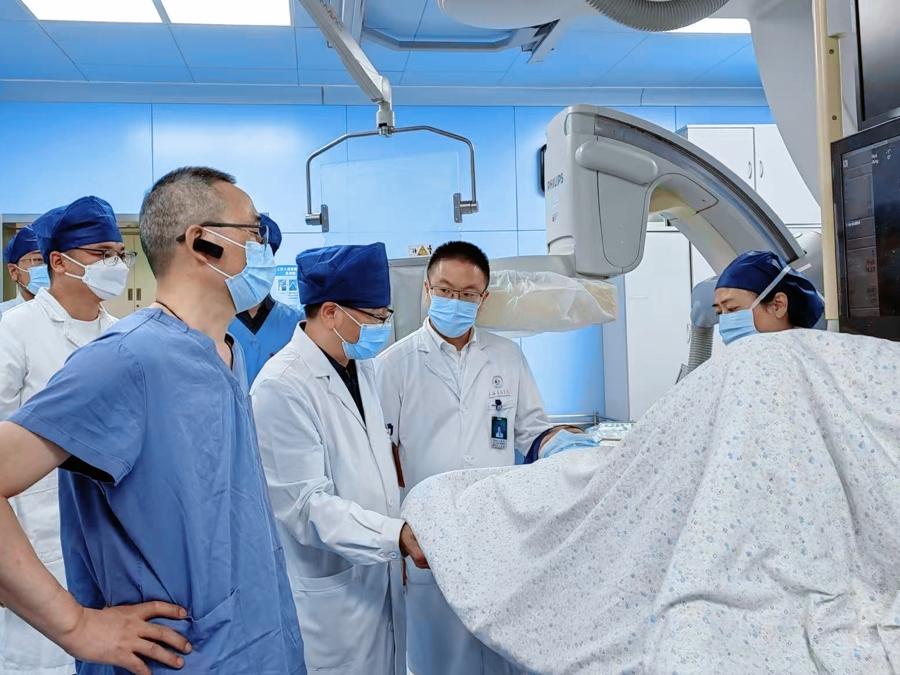
圖爲團隊正在開展再生胰島微創移植。
“首創”連連,臨牀實證“功能治癒”
殷浩和程新團隊此次共報告了3位1型糖尿病患者接受內胚層幹細胞再生胰島移植的情況,結果令人振奮。
3位患者分別爲2女1男,都長期存在血糖控制不良、頻發嚴重低血糖的情況。其中2位女性患者分別爲30歲和15歲,都是10歲出頭就確診1型糖尿病;45歲男性患者則在2019年確診。
2023年5月至2024年9月,作爲國內乃至亞洲最大的胰島移植機構之一,長征醫院分別爲他們進行了自體和異體再生胰島移植。移植手術很簡單,只需局部麻醉,然後用近似輸液的方式,將再生胰島製劑從患者肝臟門靜脈輸入,全程耗時不到半小時。手術後,3位患者的血糖控制顯著改善。特別是男性患者,術後36周起就徹底脫離胰島素,至今血糖平穩,達到臨牀治癒標準。另外2位女性患者的生活質量顯著改善。
據介紹,這3個病例涉及多個“首創”,包括世界首例自體與中國首例異體再生胰島移植治療1型糖尿病、世界首例再生胰島移植治療兒童1型糖尿病。研究團隊表示,臨牀結果在國際上首次證明,無論是自體還是異體來源的再生胰島移植,均可在1型糖尿病患者中實現胰島功能重建,從而長期改善患者的血糖水平,有效避免併發症的發生與進展。
此外,3位患者都採用了標準劑量的免疫抑制治療,用來避免移植的再生胰島被自身免疫攻擊。由於免疫抑制劑量遠小於大器官移植病人,再生胰島移植患者基本可如常人一般生活、工作和學習。實際上,傳統捐贈來源的胰島移植也需配合免疫抑制療法,其長期安全性早就經過了大量病例驗證。
一個意外發現是,30歲女性患者在術後6個月,自行停用了免疫抑制劑;雖然她移植的是自體來源的再生胰島,但依然遭遇免疫攻擊。儘管如此,這一突發情況也出人意料地證明:自體再生胰島同樣離不開免疫抑制藥物,因此,更高效、成本更低廉的異體移植,應成爲將來再生胰島治療糖尿病的主流模式。
加速成藥,最快2029年有望上市
儘管目前的成果已足夠矚目,但科學家的雄心遠不止於此。聯合團隊已錨定更高的目標——根本治癒,也就是讓患者能在移植再生胰島後,徹底擺脫免疫抑制劑。
程新告訴記者,目前他們正在緊鑼密鼓地開展下一代技術研發,將利用基因編輯技術製造“通用型”再生胰島,使它們不再被患者的免疫系統識別和攻擊。此外,新技術還將爲植入的細胞內置“安全組件”,讓醫生可在必要時“一鍵關閉”其功能,進一步提升療法的長期安全性。
在實驗室研究繼續推進的同時,團隊正努力讓這一再生胰島技術加速成爲創新藥物。據介紹,其開發的“異體人再生胰島注射液”,是目前全球唯一同時獲批中、美兩國IND的再生胰島藥物。目前一期臨牀基本完成,即將銜接後續臨牀試驗;如果一切順利,預計最快有望在2029年左右獲批上市。
程新透露,雖然現階段目標是用再生胰島治療1型糖尿病,但未來完全可以通過拓展適應症的方式,造福人數更多的2型糖尿病患者。有統計顯示,我國目前擁有全球規模最大的糖尿病羣體,患者總量約1.4億,其中1型糖尿病患者約佔5%到10%。爲了治療糖尿病及其嚴重併發症,全國每年相關總經濟負擔超過1萬億元。可以預料,隨着該項研究的不斷推進,糖尿病給無數家庭和全社會造成的沉重負擔,有望在未來持續減輕。
值得一提的是,程新所在的中國科學院分子細胞科學卓越創新中心,其前身之一中國科學院生物化學研究所等單位,曾在1965年在世界上首次人工全合成了結晶牛胰島素。殷浩所在的長征醫院,早在1976年就成功開展了首例腎臟移植。在此項研究中,雙方團隊“強強聯合”迄今已有近二十年。
在全市層面,上海近年來堅持生物醫藥“研發+臨牀+製造+應用”全過程加速、全鏈條賦能,從各個環節不斷推出新舉措,構建良好政策環境,全力打造全球“創新藥械最友好城市”。