破譯生命密碼,科學家如何從一滴血中實現癌症預警?
在醫學發展的漫長曆史中,人類一直在尋找更早、更準確發現癌症的方法。癌症之所以可怕,很大程度上是因爲早期症狀不明顯,等到出現明顯不適時,很多患者確診時往往已經錯過了最佳治療時機。據世界衛生組織統計,如果能在早期發現並治療,超過三分之一的癌症是可以治癒的,另外三分之一可以通過治療延長生命並提高生活質量。
如今,這個願景正在變爲現實。中國科學院合肥物質科學研究院核能安全技術研究所的楊良保研究員、董榮錄副研究員,聯合合肥腫瘤醫院鄧青梅等研究人員,開發出了一套革命性的智能檢測系統。這個系統結合了先進的光學檢測技術和人工智能算法,僅需一滴血液樣本,即可同步檢測六種常見的腫瘤標誌物,識別準確率達到了前所未有的100%。
這項突破性成果,標誌着我國在癌症早期診斷技術領域實現重要技術跨越。研究團隊開發的注意力尺度融合網絡(ASFN),不僅能準確識別腫瘤標誌物的種類,還能精確測量其濃度,爲臨牀醫生提供了強有力的診斷支持。
更令人振奮的是,這項技術採用的是無標記檢測方法——無需添加任何化學標記物或染料,直接對血清樣本進行分析。在傳統檢測方法中,每檢測一種腫瘤標誌物通常需要特定的試劑盒和複雜的操作流程,而這個新系統可以一次性完成多種標誌物的檢測,大大提高了效率。這意味着檢測過程更加簡單、快速,成本也更低,讓精準癌症早篩有望惠及更多人羣。
血液中的“預警信號”
我們的身體就像一座精密運轉的工廠,當某個“車間”出現問題時,便會釋放出一些特殊的“信號分子”——對於癌症來說,即腫瘤標誌物。它們就像是身體發出的求救信號,告訴我們某個地方可能出了問題。
比如,當肝臟出現癌變時,會釋放一種叫甲胎蛋白的物質;胰腺癌則會產生糖類抗原19-9;卵巢癌會分泌糖類抗原125。這些物質平時在健康人體內的血液中含量極低,一旦癌症發生,其濃度就會異常升高。醫生通過檢測這些標誌物的水平,輔助判斷患者是否可能患有某種癌症。
然而,要在血液中準確找到這些標誌物並不容易。打個比方,如果把血液比作一個巨大的游泳池,那麼腫瘤標誌物就如同滴入水中的幾滴油。要在龐大複雜的血液環境中精準捕捉微量標誌物,就需要極其靈敏和智能的檢測手段。
光的“指紋識別術”
科學家們使用了一項名爲表面增強拉曼光譜(SERS)的技術。這個名字聽起來很複雜,但原理其實不難理解。
當我們用手電筒照射一個物體時,光會被反射回來。大部分反射光的顏色沒有改變,但有極少部分光的顏色會發生細微變化。這種變化就像每個分子獨有的“指紋”,通過分析這些光學特徵,科學家就能識別出被照射的是什麼物質。
爲了讓這個“指紋”更加清晰,研究團隊使用了金納米粒子——直徑約50納米(比頭髮絲還要細上千倍)微小的金顆粒。當腫瘤標誌物分子吸附在金納米粒子表面時,會產生一種叫做“表面等離子體共振”的物理現象。簡單來說,金納米粒子就像一個超級放大器,能夠把原本微弱到幾乎檢測不到的光信號增強百萬倍以上。這就如同在安靜的房間裏說悄悄話很難被聽見,但如果拿着擴音器,即使是輕聲細語也能傳遍整個房間。金納米粒子的這種增強效應,讓科學家能夠“看見”血液中那些極其微量的腫瘤標誌物。
但新的問題又來了:血液中有成千上萬種不同的物質,它們的“指紋”相互重疊,形成了一幅極其複雜的圖像。如同在交響樂中分辨單一樂器的聲音,難度極大。
讓人工智能學會“專注”
這時候,人工智能登場了。研究團隊開發的注意力尺度融合網絡(ASFN),就像一位經驗豐富的醫生,能夠從複雜的信息中快速找出關鍵線索。
這個AI系統的工作方式很像人類的大腦。當我們看一幅畫時,不會平均地關注每個角落,而是會自動聚焦在最重要的部分。ASFN也是這樣,它會自動識別光譜中最有診斷價值的區域,忽略那些無關緊要的背景噪音。
更巧妙的是,這個系統採用了“雙管齊下”的策略。一個分支負責識別“這是什麼腫瘤標誌物”,另一個分支負責測量“濃度是多少”。就像醫生先判斷病人得了什麼病,再評估病情的嚴重程度一樣。
兩個分支還會相互“交流”。當第一個分支確定了標誌物的種類後,會把這個信息告訴第二個分支:“這是肝癌標誌物,它的正常濃度範圍是這樣的。”有了這個提示,第二個分支就能更準確地判斷濃度是否異常。
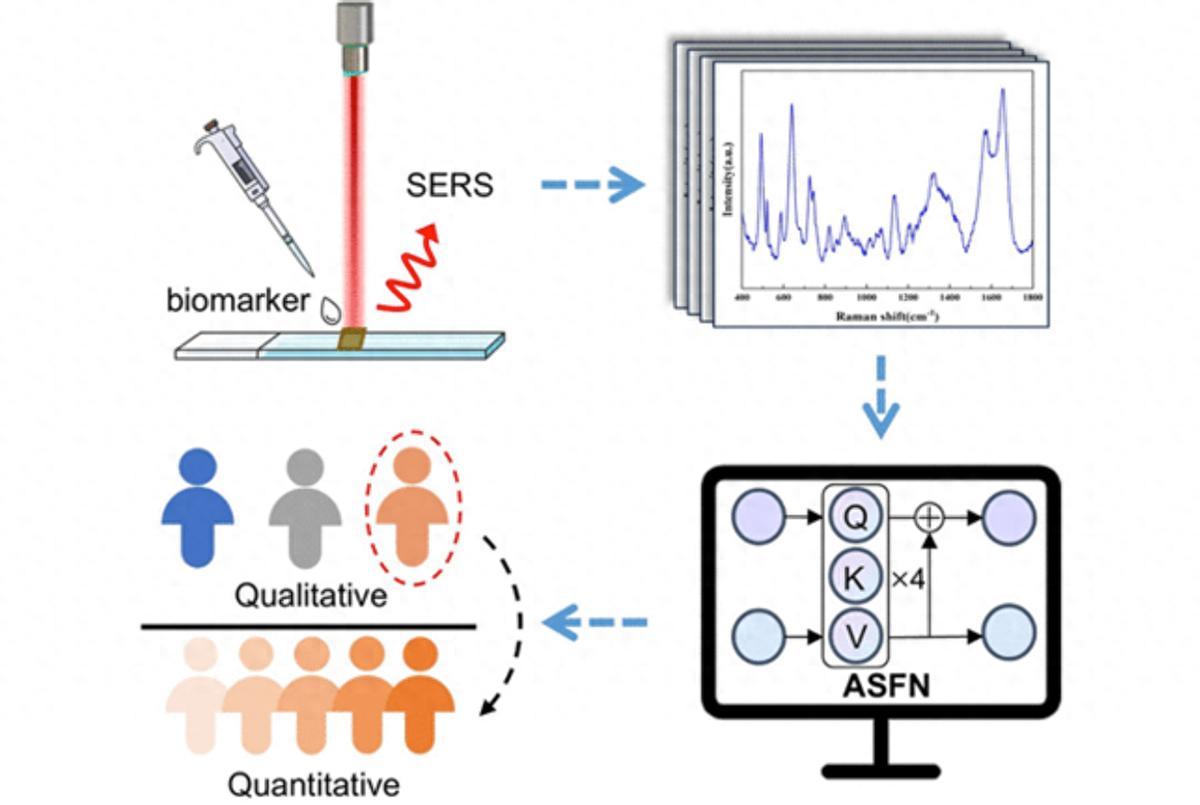
SERS 結合注意力尺度融合網絡(ASFN)用於生物標誌物的定性分類與定量預測的示意圖
(圖片來源:參考文獻1)
六種癌症標誌物的精準識別
研究團隊選擇了六種最常見的腫瘤標誌物進行測試,分別是:
癌胚抗原(CEA)——主要與結腸癌、胃癌相關,就像消化系統癌症的“哨兵”。
甲胎蛋白(AFP):肝癌的重要標誌,可以說是肝臟健康的“晴雨表”。
糖類抗原19-9(CA19-9):胰腺癌的“信使”,胰腺出問題時它會升高。
糖類抗原125(CA125):卵巢癌的“警報器”,女性健康的重要指標。
神經元特異性烯醇化酶(NSE):肺癌特別是小細胞肺癌的“信號燈”。
鱗狀細胞癌抗原(SCCA):各種鱗狀細胞癌的“標記物”。
爲了訓練AI系統,研究人員準備了4610個樣本。每種標誌物都設置了從極低到極高的15個不同濃度,尤其是在臨牀診斷最關注的“臨界值”附近,增加了更多的測試點,讓AI系統能夠牢牢掌握正常與異常的界限。
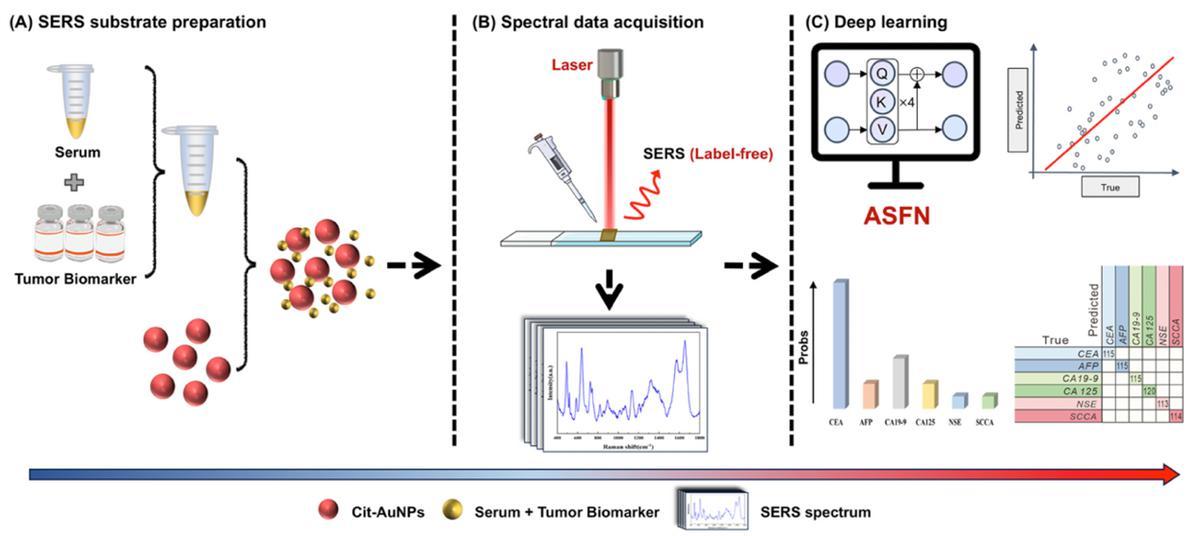
(A) 金納米顆粒的製備及其與樣品組裝用於 SERS 測量的示意圖;(B) SERS 光譜的採集;(C) 基於深度學習的腫瘤生物標誌物分類與濃度預測
(圖片來源:參考文獻1)
發現關鍵的“密碼區”
通過分析,研究團隊發現了光譜中幾個關鍵區域,這些區域如同破解腫瘤標誌物身份的“密碼”。
第一個關鍵區域(1688-1696波數)反映的是蛋白質的特徵。當這個區域的信號被屏蔽後,AI的識別準確率從100%驟降至64.74%。如同矇住了醫生的一隻眼睛,診斷能力大幅下降。
第二個重要區域(900-980波數)與細胞的能量代謝有關。由於癌細胞的代謝方式與正常細胞不同,會產生更多的乳酸等物質。這個區域就如同觀察細胞“呼吸”的窗口。
第三個區域(1428-1436波數)反映的是細胞膜的變化。癌細胞的膜結構與正常細胞有差異,這種差異會在光譜上留下痕跡。
這些發現不僅證明了AI判斷的科學性,也幫助科學家更好地理解腫瘤標誌物的特徵。
性能全面超越傳統方法
在測試中,ASFN展現出了驚人的性能。在識別腫瘤標誌物種類方面,準確率達到100%,沒有一個樣本被錯誤分類。相比之下,其他方法都有不同程度的錯誤:K近鄰算法的準確率是94.98%,隨機森林是91.54%,即使是表現不錯的卷積神經網絡LeNet-5,也有0.11%的錯誤率。
在測量濃度方面,ASFN的表現同樣出色。平均誤差只有16.89納克/毫升,考慮到檢測範圍從0到1000納克/毫升,這個誤差相當於只有1.7%,完全滿足臨牀診斷的需求。
打個比方,如果要測量一個100米長的操場,ASFN的誤差只有1.7米,而傳統方法的誤差可能達到10米甚至更多。這種精度的提升,對於早期癌症診斷來說意義重大,因爲早期發現往往意味着更好的治療效果和更高的生存率。
從實驗室到臨牀:還有多遠?
雖然這項技術在實驗室裏表現優異,但要真正應用到醫院還需要克服一些挑戰。研究團隊坦言,目前的實驗主要使用人工配製的標準樣本,真實的病人血液樣本會更加複雜。不同人的體質、年齡、其他疾病等因素都可能影響檢測結果。
此外,設備的小型化和成本控制也是需要解決的問題。目前的拉曼光譜儀還比較昂貴和笨重,要讓基層醫院都能用得起、用得方便,還需要進一步的技術改進。
但研究團隊對未來充滿信心。隨着技術的不斷進步,這種智能檢測方法有望在3-5年內進入臨牀試驗階段。屆時,一滴血、幾分鐘的檢測,就能獲得多種癌症標誌物的準確信息,爲醫生的診斷提供有力支持。
AI醫療:開啓精準診斷新紀元
這項研究是人工智能改變醫療診斷的一個縮影。通過模仿人類專家的思維方式,AI不僅能夠處理海量的數據,還能發現人眼難以察覺的細微模式。更重要的是,它能夠不斷學習和進步,積累的經驗越多,診斷就越準確。
在不久的將來,這種技術可能不僅用於癌症檢測,還能擴展到其他疾病的診斷。心臟病、糖尿病、阿爾茨海默症等疾病都有其特徵性的生物標誌物,都可能通過類似的方法進行早期篩查。
當深度學習的智慧之光照進醫學診斷的每個角落,我們有理由期待一個更加健康的未來。在這個未來裏,疾病能夠被更早發現、更準確診斷、更有效治療。
科技的進步從來都不是一蹴而就的,而是無數科研工作者日復一日的努力積累。從一個簡單的想法到成熟的技術,從實驗室的原型到醫院的設備,每一步都凝聚着智慧和汗水。但正是這些努力,讓我們在與疾病的鬥爭中不斷佔據主動,爲人類的健康事業開闢新的道路。
參考文獻:
【1】Attention Scale Fusion Network for Qualitative and Quantitative Analysis of Serum Tumor Biomarkers Via Label-Free Surface-Enhanced Raman Spectroscopy Jiawei Chen, Boyu Wu, Yanheng Huang, Yehang Wu, Shizhuang Weng, Yan Hong, Qingmei Deng, Ronglu Dong, and Liangbao Yang Analytical Chemistry 2025 97 (33), 18217-18226 DOI:
10.1021/acs.analchem.5c03263
出品:科普中國
作者:郭菲(煙臺大學)
監製:中國科普博覽