爲什麼只需改變一個質子,就能改變一個元素?
在元素週期表的118個元素中,爲什麼只需要給原子增加或者減少一個質子,元素的性質就會截然不同。
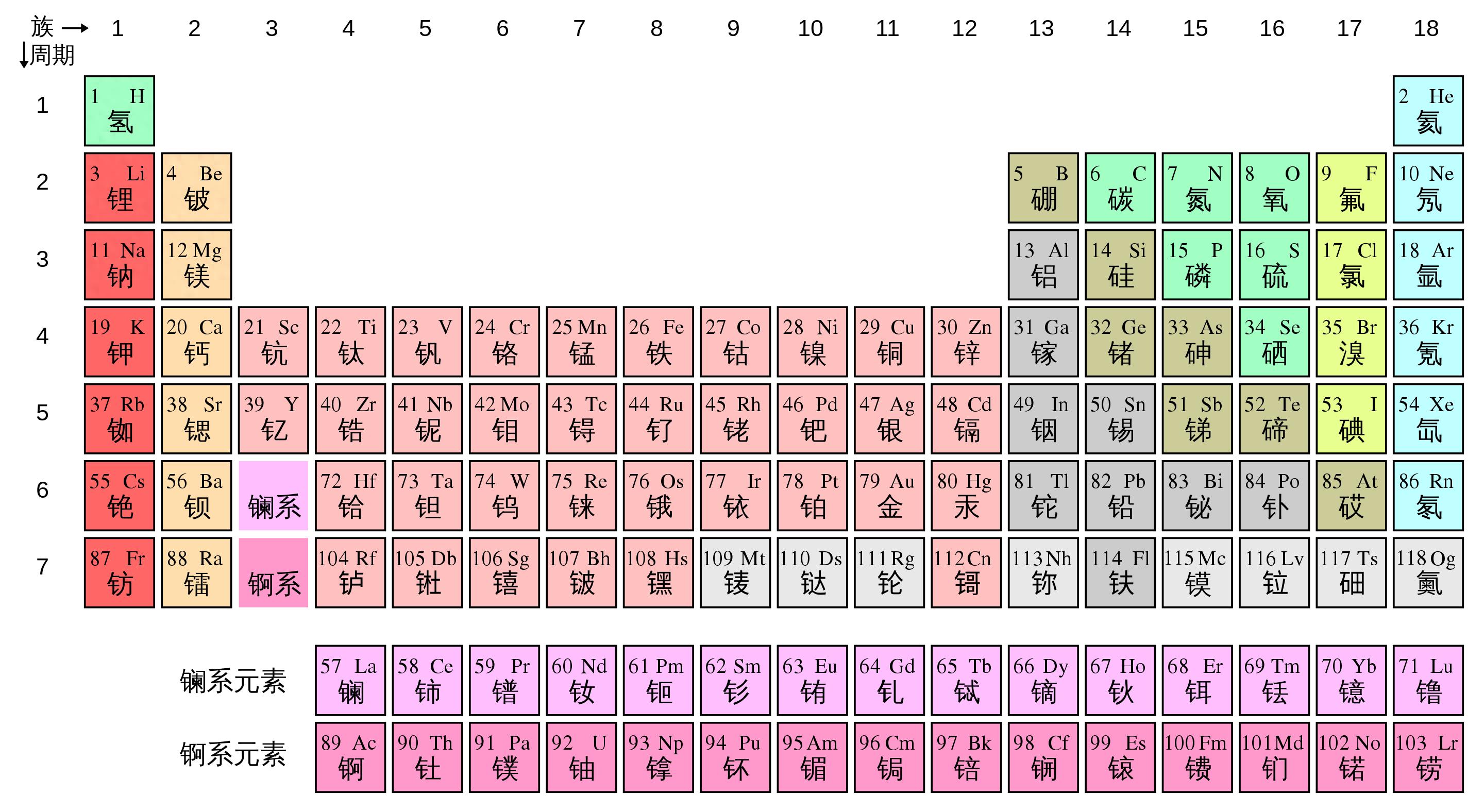
在元素週期表中,我們發現所有的元素只是原子序數不同,原子序數又取決於原子核內質子的數量。原子核中每增加一個質子,元素就會改變。這種改變甚至會造成元素的性質大變,比如以19號元素鉀爲例,它有19個質子,它在溫室的情況下是一種銀白色的金屬,質地也比較柔軟,可以輕易的用刀切割,但是它的化學活性卻很高,放在水中就會起火。因爲它會產生氫氣和大量的熱量,氫氣和氧氣結合的時候就會被點燃。

但如果只把鉀元素的一個質子拿掉,變成18個質子的原子核,這時候元素就會變成了氬,這是一種惰性氣體,性質十分穩定,它幾乎不會和其他物質發生化學反應。
但如果我們給鉀原子增加一個質子,這時候元素就變成了鈣,這是一種固體,並且比較堅硬。
在氬,鉀,鈣三種元素中,原子核的組成成分幾乎沒有區別,都是質子加中子的組合,只是質子數量改變了一個,但是化學性質卻天翻地覆。
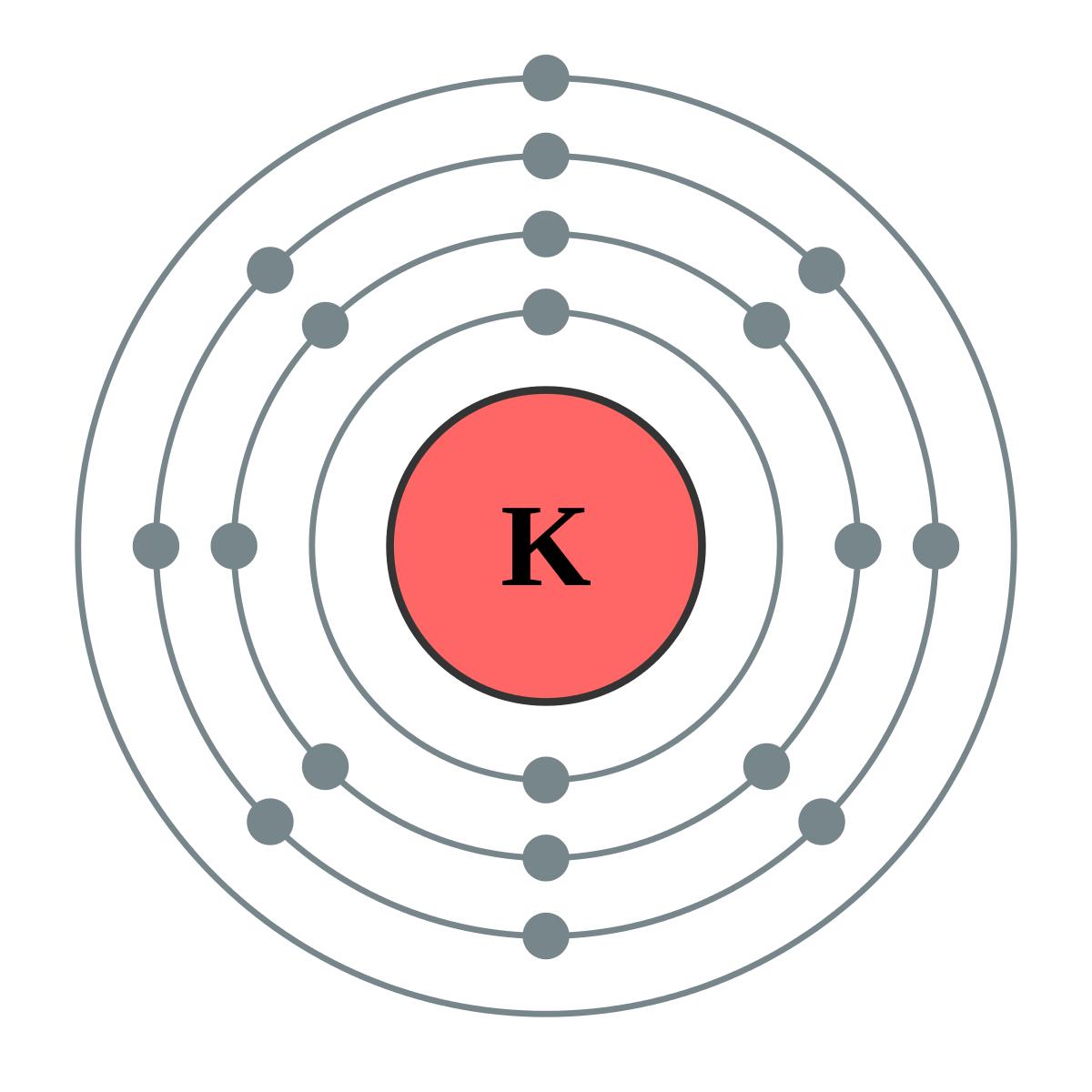
這也就是我們常說的結構決定性質。所以就有人說是質子決定了宇宙物質的種類,才使得宇宙變得如此多姿多彩。
那爲什麼質子會如此神奇呢?
首先,所有的原子都要保持電中性,我們知道原子是由原子核和核外電子構成的。原子核帶正電是因爲質子帶正電,所以原子核的電荷完全由質子決定,而原子核外又有一羣電子,電子帶負電。所以原子核要想保持電中性,整個原子內的質子數量就得嚴格的與電子數量保持同步。這樣一來,正電荷和負電荷才能抵消。所以質子數量的改變,本質改變的是核外電子的數量。而核外電子纔是決定元素化學性質的關鍵因素。

既然電子的數量纔是決定元素性質的關鍵,那爲什麼在化學課本上,我們常說原子的種類由質子決定呢?而不是直接由電子的數量決定原子序數呢?
其實這主要是因爲很多元素的核外電子並不穩定。
我們依舊以鉀元素舉例,鉀元素最外層只有一個電子,根據泡利不相容原理,同一能層的同一能級只能容納兩個電子,所以鉀原子最外層單電子就很容易與其他元素的核外電子共享同一能級。比如氯元素最外層也只有一個電子。
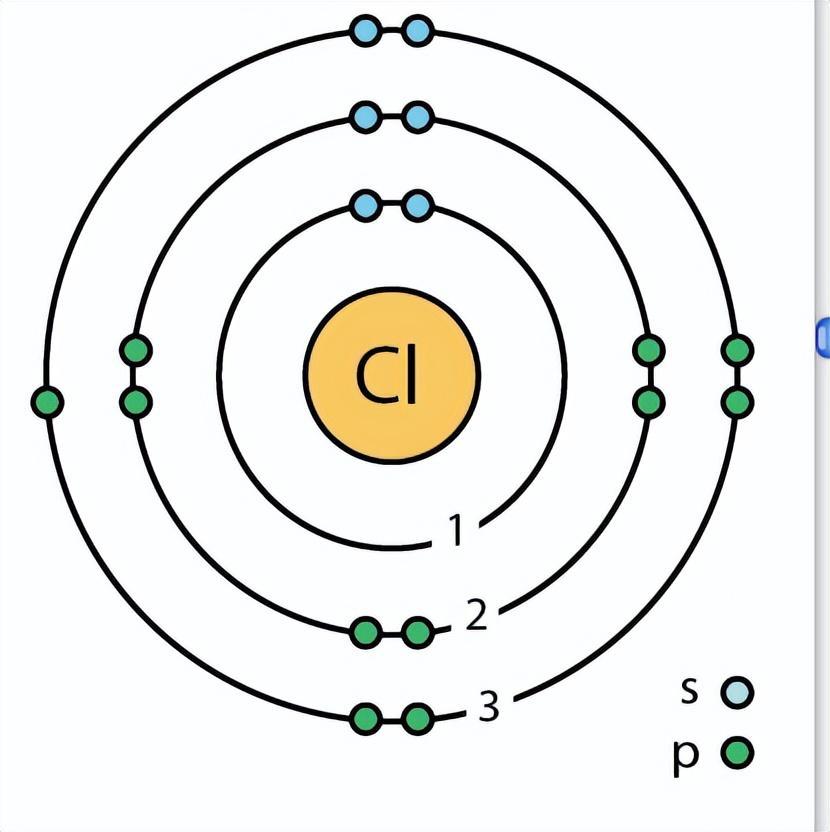
這時候鉀元素的最外層單電子很容易被氯元素的核外電子吸引過去,從而形成氯化鉀。所以鉀元素在自然界中通常以帶正電子的離子形式存在。
這個時候的鉀離子核外就只有18個電子了,其核外電子數量和氬原子數量就一樣了,即使鉀離子的電子數量相同與氬原子完全相同,但化學性質卻與氬元素完全不同。所以我們纔不能用電子的數量決定原子的種類。

看到這裏,可能會有人問,鉀元素和氯元素最外層都只有一個電子,爲什麼是氯元素把鉀元素的電子吸引過去,而不是鉀元素把氯元素的電子吸引過來呢。
其實這裏面起作用的就是能量最低原理,也就是說,核外電子一般情況下先會佔據能量最低的能級,如果最低的能級被佔滿了,纔會被迫轉移到更高的能級上。
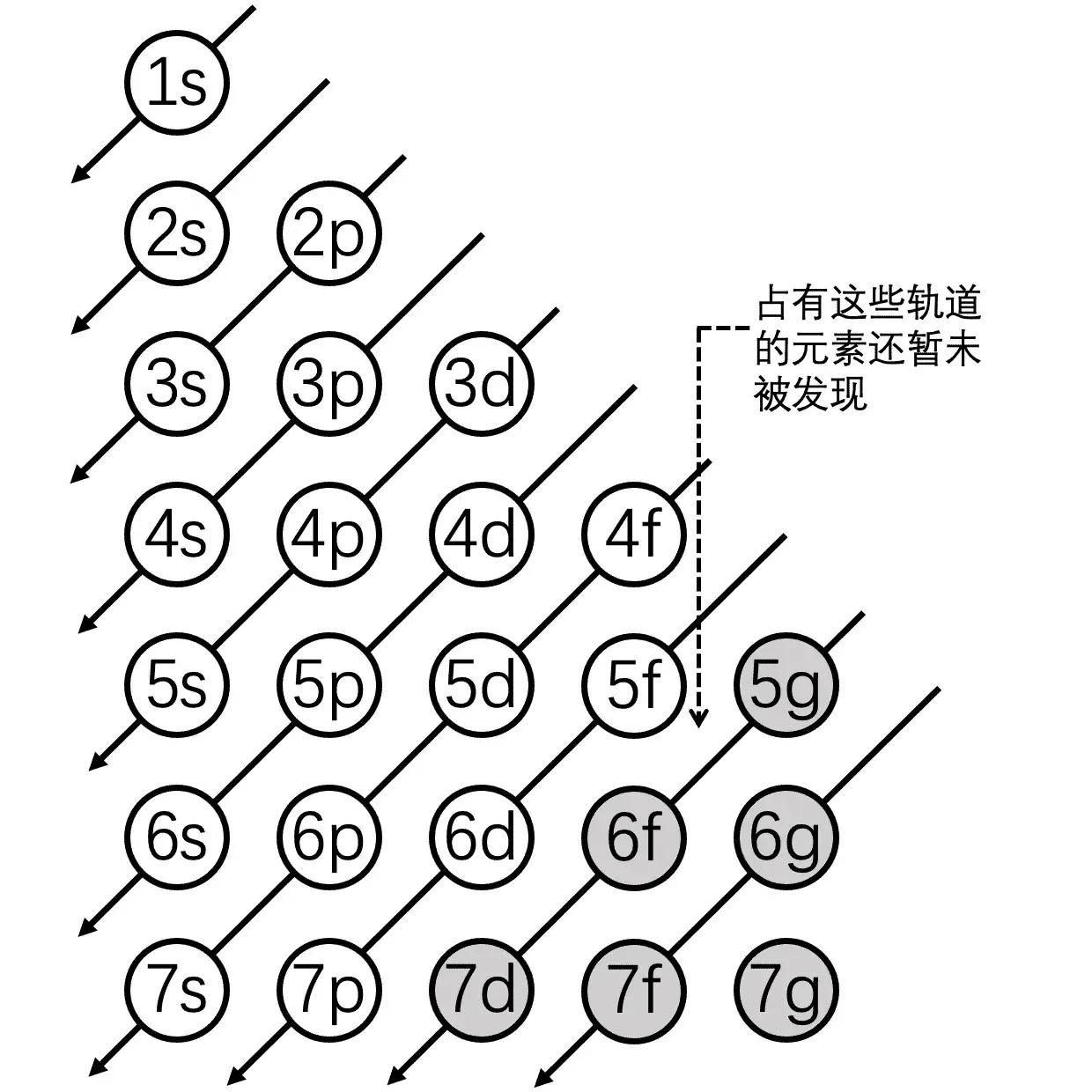
一般情況下,越靠近原子核的能層,其能量也就越低,而鉀原子的最外層單電子在第四個能層上,氯原子的最外層電子在第三個能層上。所以根據能量最低原理,是鉀元素的單電子會被氯元素拉攏過去。當然,並不是說所有的高能層的電子能級能量就一定大於低能層的能量。這裏面有一個能量交錯原理,具體情況如圖所示。
事實上,只要質子的數量不發生改變,核外電子的數量並不能直接改變元素的種類和特性。因爲核外電子數量的改變充其量也只是化學反應,而要想質子數量發生改變,就得靠衰變反應。
那什麼是衰變反應呢?
我們知道原子核的質子數量越多,其核外電子數量也就得越多,能層也就不斷增加。而能層越高,能量也就越大,那麼,要維持整個原子結構的穩定就越不容易。
而自然界的原子本質都遵守能量最低原理,電子軌道能量越低,越穩定。所以爲了維持這種穩定,原子核就會通過各種方式削減質子的數量從而減少核外電子的數量,比如通過弱力的β衰變,將質子變成中子,也就是質子中的一個上夸克通過弱力變成下夸克。這樣質子就變成中子了,由於質子數目的減少,核外電子數目也會變少,這樣整個原子結構就會變得更加穩定。
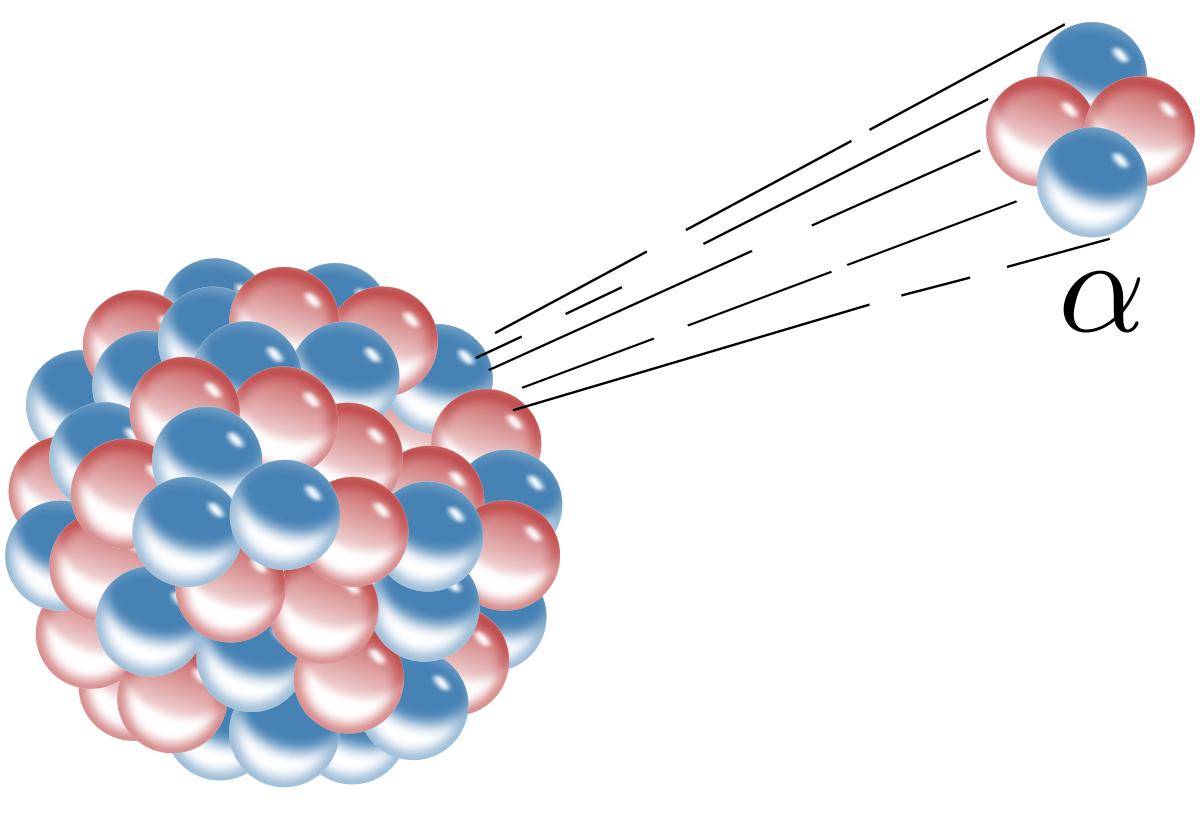
而有的時候,原子核內的質子數目實在太多,比如常見的放射性元素,只靠β衰變將上夸克變成下夸克,從而將質子變成中子的效率太低,還不足以讓原子結構快速變得穩定。這時候就得上α衰變,也就是直接將原子核中的質子和中子扔出去,一般是兩個質子和兩個中子,這也就是阿爾法粒子,即一個氦原子核。
所以說質子數量的改變只能通過衰變來改變,而質子數量直接決定核外電子的數量,而核外電子的數量決定了它們的能級分佈,這些電子在不同能級下會形成不同的化學鍵 從而決定了元素的化學和物理性質。