浙大婦院團隊《科學》發文:遠古病毒碎片竟是胚胎髮育的關鍵因素?



在生命最初的旅程中,一個受精卵需要經歷一系列精密而複雜的發育階段,才能最終成長爲一個完整的個體。然而,在輔助生殖過程中,許多胚胎在植入子宮前就停止了發育,尤其在8細胞期(8C)階段,這一發育驟停現象成爲生殖醫學領域長期未解的難題。如今,這一難題有了關鍵線索。

北京時間1月23日,浙江大學基礎醫學院/浙江大學醫學院附屬婦產科醫院研究員、長聘副教授梁洪青,浙江大學醫學院附屬婦產科醫院主任醫師、教授張丹,聯合同濟大學高紹榮院士以及浙江大學愛丁堡大學聯合學院長聘副教授劉琬璐團隊在國際頂尖期刊《科學》發表文章,首次揭示了人類基因組裏“遠古病毒化石”(內源性逆轉錄病毒,ERV),通過合成特殊的“嵌合RNA”,幫助人類早期胚胎順利跨越合子基因組激活(ZGA)關鍵發育節點。該研究不僅深化了對生命起源的理解,也爲改善輔助生殖技術提供了新思路。
臨牀之困:胚胎爲何過不了“第三天”這個坎?
“醫生,爲什麼我的胚胎總是剛開始發育就停了?”在浙大婦院生殖內分泌科的診室裏,張丹經常聽到這樣的疑問。作爲國內頂尖的生殖醫學專家,她和團隊每年要接待數千個不孕家庭,其中有一些患者會遇到早期胚胎髮育阻滯的問題——體外受精形成的胚胎,在發育到受精後第三天(8細胞階段)時,突然“卡殼”,既不繼續分裂,也無法發育爲囊胚,最終失去移植價值——這是困擾生殖醫學領域多年的“胚胎髮育阻滯”難題,也是無數不孕家庭的痛點。
“一開始,我們以爲是編碼基因出了問題。”張丹回憶道。人類基因組裏有2萬多個編碼基因,就像“生產蛋白質的說明書”,之前的研究大多認爲,若這些基因發生突變,可能導致胚胎髮育異常。

令人困惑的是,許多發育阻滯的胚胎,通過外顯組測序、家族遺傳分析等檢查方式,並未發現編碼基因有特別異常——染色體沒問題,已知的與早期胚胎髮育相關的基因突變也未出現,可胚胎就是“活不下去”。“我們無法解釋這一現象。這種‘無解’的狀態,對醫生和患者都是一種煎熬。”張丹說。這也讓研究團隊陷入思考:難道基因組裏還有未知領域在影響胚胎髮育?
與梁洪青團隊的碰撞,爲這個問題帶來了新視角。2019年,長期研究幹細胞與轉錄調控的浙江大學基礎醫學院研究員梁洪青雙聘到浙大婦院,與張丹團隊頻繁交流學術問題。“基因組裏非編碼區還有超過40%的 ‘暗物質’——逆轉座子序列,其中內源性逆轉錄病毒(ERV)是一個重要的分支。”梁洪青說,ERV是遠古病毒感染人類祖先留下的“基因化石”,雖然大多失去了感染能力,但可能在進化中被“馴化”,參與生命活動。
與此同時,研究人員觀察到,在人類體外受精胚胎的8細胞“瓶頸期”,胚胎想要繼續往下發展,需要一股“洪荒之力”——成功啓動自身的基因表達程序,即“合子基因組激活”(ZGA),這樣才能實現從依賴卵子儲存的母源物質到激活自身基因組的切換。ZGA如同生命啓動的“總開關”,一旦失敗,胚胎髮育便會阻滯於此。
“已知的、負責編碼蛋白質的基因中,僅有少數幾十個被發現與早期胚胎髮育調控直接相關。對於大量臨牀上找不到編碼基因突變的發育阻滯案例,我們推測,問題的答案可能隱藏在佔據基因組絕大部分、功能未知的‘非編碼區’。”張丹解釋道。
臨牀的迫切需求與基礎研究的探索在此交匯,雙方都覺得這是一個很有意思也很有想象力的好問題。團隊決定從合子基因組階段特異性高表達的ERV入手,對比正常胚胎和發育阻滯胚胎的差異。結果令人驚喜:在發育阻滯的8細胞胚胎中,ERV家族裏的MLT2A1的亞家族,表達量比正常胚胎顯著下調!“這似乎找到一個關鍵線索——MLT2A1的‘缺席’,可能正是胚胎‘卡殼’的原因。”梁洪青表示。由此,團隊鎖定了進一步的研究目標:探索MLT2A1如何影響胚胎髮育。
創新突破:“遠古病毒化石”變身,解鎖胚胎啓動的3大密碼
要弄清楚MLT2A1的作用,首先得看清它在胚胎裏“做什麼”。團隊採用了納米孔長讀長測序技術——相當於給RNA拍“全身照”,能完整讀出它的序列,不遺漏細節。該技術的應用帶來了第一個重大發現:MLT2A1在ZGA階段並非孤立地表達自己,而是主動地與下游各種不同的基因組序列“手拉手”融合,形成了一系列結構特殊的“嵌合RNA”。
“這徹底顛覆了我們的認知。”論文共同第一作者、浙大婦院博士後向陽泉感嘆,“就像一把鑰匙,原本只有一種齒形,卻能搭配不同的‘齒套’,變成無數種鑰匙。”研究結果顯示,MLT2A1的“主體”是固定的,但會和下游的編碼基因、非編碼序列,甚至其他逆轉座子融合。研究人員在人類8細胞期胚胎和幹細胞中鑑定出幾百種不同的嵌合轉錄本,這些嵌合RNA平均長度在500-1000鹼基之間,絕大多數通過剪接事件連接而成。
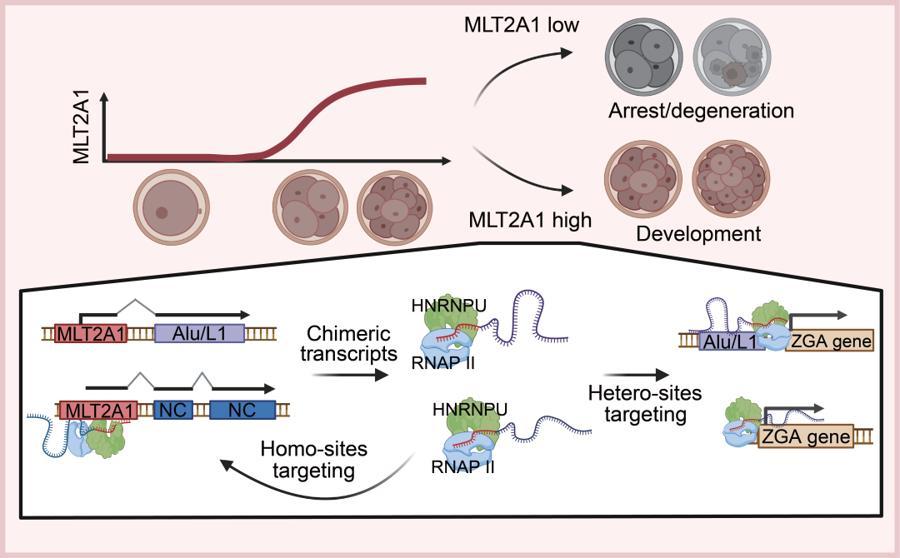
MLT2A1 亞家族逆轉座子調控胚胎合子基因組激活的示意圖
這意味着,MLT2A1通過這種廣泛的“嵌合”模式,極大地拓展了其RNA序列的複雜性和多樣性。原本只有3800多種相似“鑰匙”,現在變成了能打開基因組中成千上萬把不同“連環鎖”的“萬能鑰匙串”。
那麼,這些“嵌合RNA”如何具體行使功能?研究團隊揭開了第二個關鍵機制:MLT2A1 RNA主要富集在細胞核內。在同濟大學高紹榮院士的支持下,團隊揭示了它們利用其嵌合特性,能夠精準地靶向並結合到基因組上大量與ZGA相關的位點。
更關鍵的是,MLT2A1 RNA並非“單打獨鬥”。它通過其保守的序列區域,招募了一個重要的核內蛋白“幫手”——HNRNPU。兩者形成的複合物,又能進一步招募負責基因轉錄的“核心機器”——RNA聚合酶II。
“它們就像一組緊密咬合的‘命運齒輪’,”張丹形容,“一個齒輪轉動,會帶動周圍所有齒輪一起轉動。這種自我放大和集體行動的機制,確保了在ZGA這個關鍵時間窗口,能夠快速、強勁地啓動全局性的基因表達程序,幫助胚胎順利跨越發育瓶頸。”
價值深遠:不止於“讀懂”胚胎,更打開生殖健康新視野
從門診中碰到早期胚胎髮育阻滯的病例,到臨牀與基礎研究團隊互相啓發擦出創新的火花,在張丹和梁洪青看來就像是一個偵探破案的過程,“浙江大學和浙大婦院都有着交叉創新與開放合作的科研氛圍,不同研究背景的專家是真正的‘人在一起’地工作,擴大了各自的研究領域。”而這項融合了基礎和臨牀的研究,意義也是多重的。
首先,它深化了我們對生命起源的理解。研究首次令人信服地揭示,曾被忽視的基因組“暗物質”——內源性逆轉錄病毒,在人類生命最初的塑造過程中,扮演了積極主動且至關重要的角色,爲發育生物學提供了全新的認知視角。

其次,它爲改善輔助生殖技術提供了全新的科學思路和潛在的未來路徑。張丹表示:“未來,如果能通過對MLT2A1等分子的檢測,更早、更精準地預測胚胎活力,將有助於我們篩選出最優質的胚胎進行移植,從而提高試管嬰兒的成功率。”
另一方面,這項研究爲理解並干預因ZGA失敗導致的胚胎髮育阻滯奠定了一定的理論基礎。張丹表示,“未來或許可以通過優化體外培養體系,模擬更接近體內的環境,來更好地支持胚胎自身基因組的激活程序,幫助更多胚胎順利發育。”
當然,研究人員也強調,從基礎研究的突破到真正的臨牀應用尚有很長的路要走。未來,浙大婦院的研究團隊將繼續深入研究,努力爲衆多遭受不明原因胚胎髮育阻滯困擾的家庭提供未來希望。