復旦團隊開發腫瘤邊界可視技術,不用造影劑,爲手術精準導航


在外科手術中,如何在術中實時、準確判斷腫瘤邊界,是影響手術切除效果和患者預後的關鍵因素之一。真實臨牀場景下,外科醫生往往難以僅憑肉眼觀察和觸診等常規方法對腫瘤邊界作出精準判斷。術中病理檢查雖然能夠對局部組織進行良惡性定性分析,但存在耗時較長、取樣範圍有限等弊端。因此,開發一種安全、快速、可靠的術中腫瘤邊界可視化技術,始終是精準外科領域亟待解決的問題。
近日,復旦大學張凡/何海生團隊聯合附屬華山醫院欽倫秀/朱文偉團隊,成功創制了一種無需注射任何造影劑的術中實時腫瘤邊界可視化新技術,即組織自發熒光近紅外成像技術(TANI)。該技術通過利用組織內源性熒光物質在近紅外二區(NIR-II,1000-1700 nm)的信號差異,實現了多種肝臟惡性腫瘤邊界的清晰、高對比度可視化,並有效避免了血液和膽汁污染、肝硬化背景以及良性病竈帶來的干擾。研究團隊進一步於多例患者體內驗證了該技術在外科手術導航中的應用潛力,爲肝臟惡性腫瘤的精準切除提供了全新的臨牀輔助手段。
1月20日,相關研究成果以《無標記組織近紅外二區自發熒光成像技術用於人肝惡性腫瘤可視化》爲題,在線發表於《自然·生物醫學工程》。
據研究團隊介紹,目前臨牀常用的術中腫瘤可視化方法主要依賴外源性造影劑的使用。該方法需要在術前向患者體內注射吲哚菁綠(ICG)等造影劑,通過該分子在腫瘤組織中的富集實現熒光引導手術。然而,ICG在部分患者中可能引發過敏等不良反應,更重要的是,該造影劑容易在非腫瘤組織(如肝硬化組織或膽汁淤積區域)中非特異性聚集,導致假陽性信號,臨牀報道的誤判率可高達40%,顯著降低了術中判斷的可靠性。
針對上述問題,研究團隊提出利用人體組織中本身存在的內源性熒光信號,在無需注射外源造影劑的前提下實現腫瘤可視化,從而有效規避造影劑帶來的安全性隱患及脫靶干擾。通過對大量臨牀組織樣本進行系統性自發熒光分析,團隊發現了一種近紅外發光的內源性物質,其在>1000 nm波段的信號可以很好的區分惡性腫瘤和正常組織。

TANI技術光路示意圖及其用於牀邊可視化肝惡性腫瘤的工作流程圖
基於這一發現,研究團隊進一步開發並優化了針對該內源性熒光物質的成像技術與參數設置,形成了TANI成像體系。在該技術下,正常肝組織呈現均一而明亮的近紅外熒光信號,而腫瘤區域表現爲顯著減弱甚至缺失的熒光信號,二者對比度高,腫瘤邊界直觀清晰。特別對於肉眼無法識別的腫瘤,TANI技術能夠清晰、準確探測出該腫瘤邊界。
研究結果表明,TANI技術在肝細胞癌、肝內膽管癌以及多種肝轉移腫瘤(包括結直腸癌、胃腺癌和乳腺癌肝轉移等)中均表現出穩定、優異的腫瘤邊界可視化能力。同時,該技術對不同分化程度、病竈大小和臨牀分期的腫瘤均具有穩定的成像效果,即使在肝硬化等複雜病理背景下,仍能實現清晰、可靠的腫瘤可視化,展現出良好的臨牀適用性。此外,即便在術中不可避免出現血液或膽汁污染的情況下,該技術依然能夠提供清晰、可靠的成像結果。
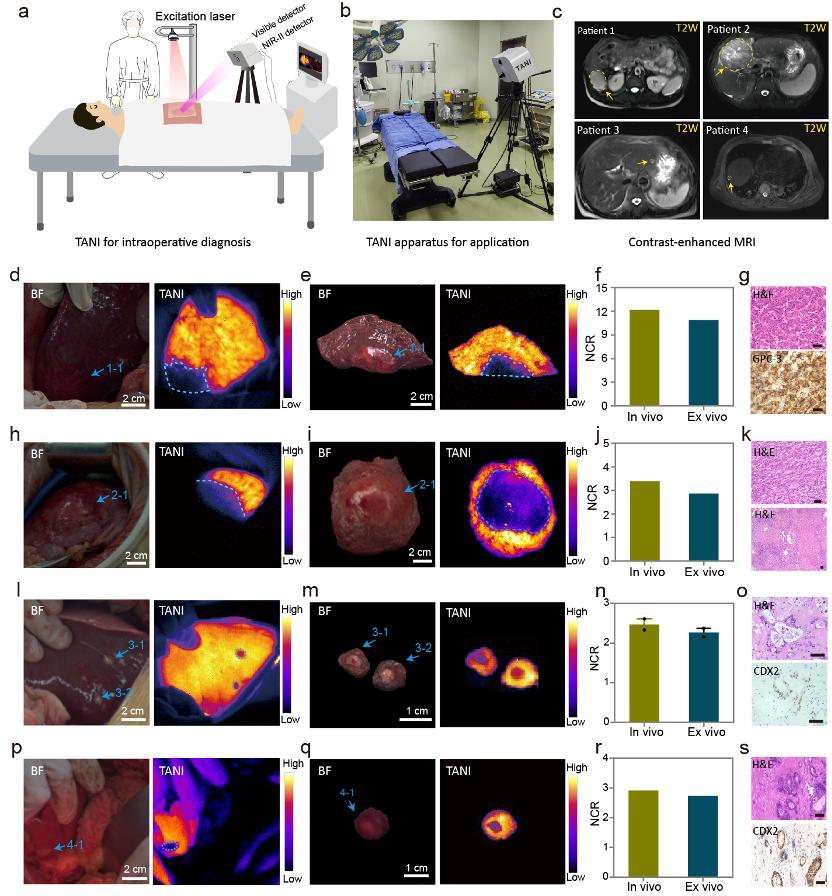
TANI技術於患者體內實時可視化肝惡性腫瘤的流程、裝置與效果圖
在獲得倫理許可後,研究團隊將TANI技術應用於真實術中場景,在多例肝切除手術中成功實現了對原發性肝細胞癌及多髮結直腸癌肝轉移竈的實時識別。在腫瘤切除完成後,TANI還可用於對手術切緣進行快速掃描,輔助判斷是否存在殘餘腫瘤組織,爲實現“精準切除、降低復發風險”提供了重要支持。術後病理檢查結果與術中成像高度一致,進一步驗證了該技術的臨牀可靠性。
作爲一種無標記、非接觸、寬視場、實時的術中成像技術,TANI操作簡便、成像信息直觀,可作爲現有熒光引導手術的重要補充手段,有望在肝臟腫瘤等外科手術中發揮重要作用。未來,隨着多中心臨牀研究的深入開展以及成像設備的進一步優化,該技術有望爲更多患者帶來更加安全、精準的手術治療體驗。同時,進一步闡明該內源性熒光物質的分子基礎及形成機制,不僅有助於深入理解腫瘤等疾病的發生發展,還可能爲這些疾病的早期識別與精準調控提供新的研究方向。
復旦大學藥學院青年副研究員何海生、華山醫院肝膽外科主任醫師朱文偉爲共同第一作者;化學系教授張凡、華山醫院普外科教授欽倫秀爲通訊作者。研究工作由化學系、藥學院、華山醫院、聚合物分子工程全國重點實驗室、智能化遞藥教育部重點實驗室與克服遞藥屏障高端製劑全國重點實驗室成員共同完成,並獲得了國家重點研發計劃、國家自然科學基金委員會、科學探索獎、新基石科學基金會、上海尚思自然科學研究院、上海市科學技術委員會、上海市教委創新計劃等機構與項目的大力支持。