有望終結打針煎熬?浙大“快遞員” 可帶胰島素無創透過皮膚吸收



糖尿病人的胰島素治療,有望扔掉針頭了!
據國際糖尿病聯盟估算,2024年全球20-79歲糖尿病患者約爲5.89億,其中1型糖尿病與晚期2型糖尿病患者都長期依賴胰島素,且都需通過注射給藥,有的一天需要打3到4針,令患者身心都承受着巨大壓力。100年來,無數科學家試圖打破胰島素需要注射這一“魔咒”,但都鎩羽而歸。
近日,浙江大學團隊牽頭在國際頂刊《自然》發表了題爲《一種用於無創透皮胰島素遞送的皮膚滲透性高分子》(A skin-permeable polymer for non-invasive transdermal insulin delivery)的研究,首次提出用一種皮膚滲透性高分子——聚[2-(N-氧化物-N,N-二甲基氨基)乙基甲基丙烯酸酯](OP),成功實現胰島素無創透皮給藥,其胰島素鍵合物(OP-I)在糖尿病動物模型中,表現出與皮下注射胰島素相當的降糖療效,給糖尿病人帶來了新希望。

這種高分子聚合物,可以透過皮膚
早在胰島素分離成功的第二年(1922年),人類就已經開始研究胰島素口服制劑了。如果胰島素不用注射,不僅更方便、痛苦少,還可減少大量針頭和注射器報廢形成的醫療垃圾,是顯而易見的更優選擇。
但是100年過去了,胰島素只能注射給藥的“魔咒”一直未能改變。浙江大學團隊這次的突破性發現,就有望通過透皮給藥打破這一“魔咒”。
皮膚角質層作爲人體隔絕外界物質的第一道保護屏障,其中角質細胞與脂質的有序排列形成緻密結構;緊鄰其下的活性表皮層中細胞間緊密連接,構成了一道堅固的皮膚“城牆”。
透皮給藥歷史悠久,早在古代,人們就通過膏藥外敷的方式治療疾病。目前部分麻藥、心血管疾病等小分子藥物也實現了無創透皮給藥。但目前僅有少數特定結構的小分子能穿透皮膚。胰島素等生物大分子,因分子量大、結構複雜,難以突破皮膚壁壘,這也成爲透皮遞藥研究的核心難點。
過去,人們嘗試過微針刺破皮膚、超聲波震盪、甚至用化學藥劑強行突破皮膚角質層。這些方法雖然有效,但往往伴隨着疼痛、皮膚損傷和感染風險。

在前期的相關研究中,論文通訊作者、浙江大學化工學院申有青教授團隊發現了一種兩性離子聚合物OP,它在腫瘤組織中具有出衆的滲透性,能夠高效遞送抗腫瘤藥物。
“由此,我們猜測,OP是否也能高效地滲透皮膚組織呢?”這個靈光一現的想法,讓長期專注高分子藥物遞送研究的申有青,敏銳捕捉到了潛在的研究方向。
果然,隨後實驗中,OP在皮膚上也表現出高滲透性,讓團隊成員倍感驚喜。“這打破了我們對‘大分子無法透過皮膚屏障’的常規認知。”申有青表示,團隊隨即聯合浙大生命科學學院教授周如鴻、英國帝國理工學院教授陳榮軍團隊,展開系統研究,深入分析OP透過皮膚的具體路徑和機制,進一步探索它在透皮給藥領域的應用可能。
胰島素有了“快遞員”
OP到底是怎樣突破皮膚屏障,幫助大分子胰島素進入人體內循環的?其實,這與皮膚的pH有關。
團隊發現,皮膚從表面到內部,呈現從酸性環境到中性環境的天然pH梯度,OP正是利用這一特性,通過動態調整自身帶電形態,進行巧妙滲透。
首先,OP含有的三級胺氧化物基團,在皮膚表面(皮脂膜及角質層表層)pH≈5的弱酸性條件下,發生質子化,帶上正電。通過靜電相互作用,OP與角質層細胞間隙帶負電的脂肪酸緊密結合,形成局部高濃度藥物儲庫,爲後續滲透提供濃度梯度。
隨着滲透深度增加,角質層內側至活性表皮層的pH升至中性,OP發生去質子化,轉變爲電中性且親水的聚兩性離子,此時它失去與角質層脂質的靜電相互作用,得以快速擴散通過角質細胞間隙,實現高效滲透。

OP-I在皮膚角質層擴散的分子動力學模擬。
“我們通過分子動力學模擬與結合自由能計算,從原子層面闡明瞭這一適配皮膚生理pH梯度的智能遞藥機制。”周如鴻介紹。
團隊將OP與胰島素化學偶聯,構建出鍵合物OP-I。進入活性表皮層及真皮層後,OP-I沿細胞膜表面發生“跳躍式移動(hopping)”,避免胰島素被細胞內的酶降解。這種“跳躍遞送”透過深層皮膚後,最終經真皮層淋巴管進入體循環,實現了胰島素的全身遞送。這就像是讓OP這個可以靈活變形的“快遞員”,帶着胰島素“包裹”鑽過皮膚“城牆”,遞送至血液中。
有望爲多種慢性疾病提供治療新方案
爲驗證該透皮給藥技術的有效性與安全性,研究團隊在兩種糖尿病模型動物中開展評估。結果表明,OP-I能高效靶向肝臟、脂肪、肌肉等血糖調控關鍵組織,爲其強效降糖效應提供了明確機制支撐。
具體而言,對STZ(鏈脲佐菌素,一種常見誘導素)誘導糖尿病小鼠經皮給予116U/kg OP-I,血糖在1h內即可快速降至正常範圍,降糖效果與皮下注射胰島素相當,藥效持續時間延長至12h以上且無低血糖風險。SPR(表面等離子體共振)實驗進一步表明,OP-I與胰島素受體的結合能力與天然胰島素相當;對於皮膚結構更接近人類的糖尿病迷你豬,僅需29U/kg的經皮給藥劑量,即可實現血糖正常化。
不同於傳統化學促滲劑的屏障破壞,OP-I持續給藥後,動物皮膚角質層結構完整、細胞間隙無擴張,也沒有出現炎症等副作用。毒性試驗表明,OP同樣具備極高的體內安全性。隨着臨牀研究的持續推進,未來可能只需通過皮膚塗藥便可實現血糖平穩控制,顯著提升治療效率。對糖尿病患者而言,“告別針頭”將不再是奢望。
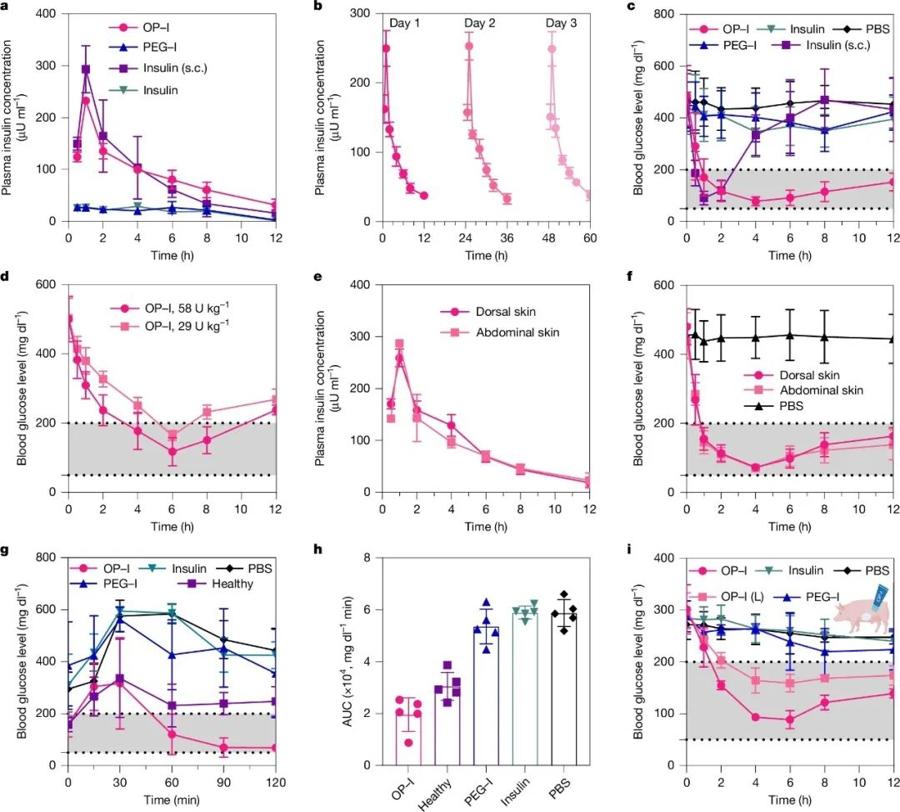
OP-I經皮給藥後的降糖效果。
“更重要的是,我們這個技術平臺不僅適用於胰島素遞送,還能用於其他重要的生物大分子。”申有青介紹,目前,該體系已成功拓展至利拉魯肽、司美格魯肽、治療性蛋白、單克隆抗體及siRNA(小干擾核糖核酸)等多類物質的遞送。
目前,相關技術已轉讓企業並推進臨牀轉化,不僅有望重構生物大分子給藥體系,更能爲糖尿病、類風溼關節炎等需長期注射的慢性疾病提供創新治療方案。
浙江大學化學工程與生物工程學院博士後韋秋雨、生命科學學院博士後何至、化工學院博士生李梓凡、教授周珠賢爲共同第一作者,浙江大學化工學院教授申有青、生命科學學院教授周如鴻,英國帝國理工學院教授陳榮軍及浙江大學化工學院研究員相佳佳爲共同通訊作者。