睡不好的人開始嗑鎂片了,但有人喫了可能會死
⚠️利益衝突聲明:
本文寫作過程裏沒有得到任何來自鎂補劑廠家的經濟支持或干擾。
⚠️本文的使用方式:
想象你的身體是一棟房子。如果你每天都往房子裏丟垃圾(營養不均衡,熱量超標),丟垃圾(沒有堅持運動),丟更多垃圾(沒有良好和充足睡眠),甚至有時候在房子裏點火(抽菸酗酒)……
然後,你僱了一個清潔工(補劑、某種抗衰方法),每天來工作一小時。
清潔工或許有用,但不一定趕得上你丟垃圾的速度。
在這種情況下購買補劑/抗衰方法,可能買的只是一種微小的、膠囊狀的希望,以及比其他人更昂貴的尿液。
如果你不想放棄精緻碳水,不想放棄躺着耍手機的快樂,不想放棄熬夜時一個人的寧靜,不想放棄偶爾微醺的快樂……總之,你拒絕改變任何一項不良生活習慣。
你需要知道,在一個充滿糖分、酒精和久坐的生活方式中投入補劑,就像是試圖用一卷膠帶去修復泰坦尼克號的船體,或者用一杯水去澆滅燃燒着熊熊大火的房子。
在充分理解了以上信息後,如果你還是想繼續往下讀。那就讀吧,因爲作者本人也是這樣的。
在當下,大部分人都不缺喫不缺穿,但擁有充足睡眠的打工人就像綠孔雀一樣罕見。
關於“改善睡眠”的補劑, 也是滿坑滿谷。其中一個,是一種金屬——鎂。

鎂片可以改善睡眠嗎?爲了回答這個問題,我在論文的海洋裏撈了半天,試圖搞清楚這種金屬元素到底在我們的身體裏做些什麼。
缺鎂,對睡眠不好
先明確一點,鎂不僅僅是某種你會在複合維生素瓶子背面看到的無聊“礦物質”。它是人體內第四大陽離子,影響着超過600種酶促反應,是細胞生化反應的基礎底座。如果你的身體是一個繁忙的建築工地,鎂就是那個拿着對講機、確保每個人都在正確時間正確地點幹活的工頭。
在睡眠優化中,鎂理論上可以通過三條路徑發揮作用。
第一條路徑涉及大腦裏的 NMDA受體。在這裏,鎂離子充當了“看門人”的角色,堵在NMDA受體通道門口,防止鈣離子過度湧入神經元,造成神經元過度興奮。簡單來說,鎂就是大腦的強制冷靜劑。
第二條路徑是關於下丘腦-垂體-腎上腺軸(HPA軸)的。鎂在這裏能減少促腎上腺皮質激素(ACTH)的釋放,直接從源頭降低夜間皮質醇水平——這個壓力荷爾蒙經常讓我們臨入睡前突然驚坐而起“不是,我當時有病吧!”,並在凌晨三點盯着天花板思考人生的起起落落落落落落落落落落。如果你經常在夜裏翻來覆去反芻過往,你可能就需要鎂來幫忙調低自己的“皮質醇覺醒反應”。
第三條路徑涉及GABA,一種讓你放鬆的神經遞質。鎂不僅踩了興奮的剎車(NMDA),還踩了睡眠的油門(GABA)。鎂是GABA受體的激動劑,能增強GABA功能,直接誘導放鬆和慢波睡眠 。從這個角度講, 與GABA有關的補劑比如茶氨酸,可以和鎂一起產生助眠的協同效應。
總之,鎂很重要,鎂對良好睡眠也很重要。
如果你喫得健康均衡,比如餐桌上天天擺滿了綠葉菜粗糧和豆類,營養充足不缺鎂,那麼一切都很好。
江蘇的隊列研究(Zhang et al., 2018)就發現,高鎂攝入與女性白天嗜睡風險降低顯著相關(OR=0.12)。這意味着,如果你攝入足夠的鎂,你就不太可能在下午三點的會議上睡得像個點頭娃娃。
但如果你缺鎂,就不太妙了。
觀察性研究表現出了驚人的一致,比如美國的NHANES、CARDIA,以及中國的江蘇營養研究,都一致指出:飲食中鎂攝入不足與睡眠短、炎症高、以及睡眠呼吸暫停(OSA)風險增加高度相關。
而且還有個惡性循環。
當你感到壓力時,你的身體會做出一個令人費解的決定:它開始瘋狂地通過尿液排出鎂。
而且,當你因爲壓力大而睡不着時,你不太可能半夜起來水煮一盤富含鎂的菠菜,你更可能撕開一袋薯片嚼嚼嚼(然後高鹽就會促使腎臟排出更多的鎂)。
然後鎂缺乏會讓你對壓力更加敏感,導致 HPA 軸過度激活,皮質醇水平飆升,從而讓你感到 更多 的壓力,進而尿出更多的鎂。
NHANES數據顯示,短睡眠(<7小時)人羣的鎂攝入顯著低於正常睡眠者。
江蘇隊列顯示,基線鎂攝入低的人,5年後睡眠障礙風險上升。
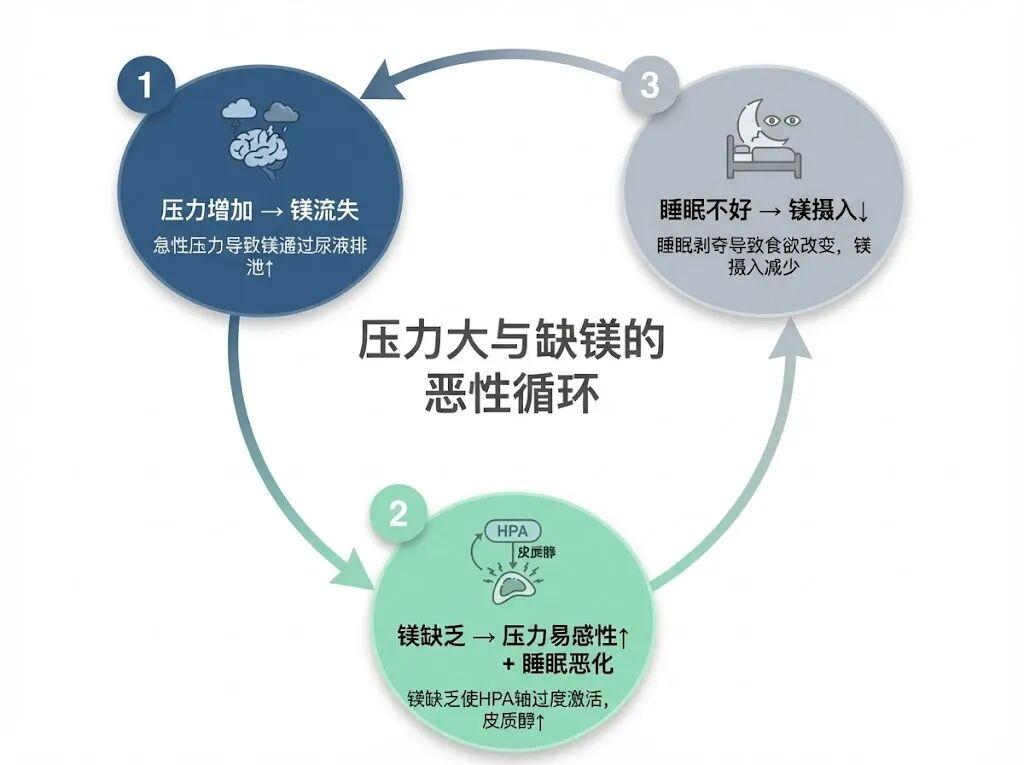
總之:
1️⃣壓力 → 鎂流失:急性壓力導致鎂通過尿液排泄↑。
2️⃣鎂缺乏 → 壓力易感性↑+睡眠惡化:鎂缺乏使HPA軸過度激活,皮質醇↑。
3️⃣睡眠不好 → 鎂攝入↓:睡眠剝奪導致食慾改變,鎂攝入減少
嗑鎂片,效果怎麼樣?
嗑鎂片的干預性試驗(RCTs),結果大概如下:缺鎂的人羣補鎂可以改善睡眠。但對於那些健康的、鎂充足的人羣,補鎂的效果經常被證明“與安慰劑無差異”。
Held 在2002 年的一項研究中,健康老年受試者的慢波睡眠(SWS),也就是那種真正讓人恢復精力的深度睡眠,從10.1 分鐘增加到了 16.5 分鐘。你可能覺得這聽起來不多,但深度睡眠隨着年齡增長會急劇減少,對於那些拼命想在淺眠的海洋中抓住一點深睡浮木的老年人來說,每天增加63%的深睡眠時間聽起來還是很誘人的。
皮質醇也確實改善了。Abbasi 在 2012 年的研究發現,對於老年失眠患者,補鎂在改善睡眠質量的同時,確實顯著降低血清皮質醇(p=0.008),同時提升了褪黑素水平(p=0.007)。這意味着鎂確實調低了身體的壓力反應。

不過,接下來要講缺點了。
鎂片主要改善的是主觀感受(你覺得你睡得好了)、入睡潛伏期(你更快睡着了)和慢波睡眠。
主觀感受很容易受到干擾。安慰劑效應、期望偏倚(“我花了大價錢買這個,它必須有效”),以及回憶偏倚,都會影響數據。雖然有些研究在做雙盲或者單盲,但是從腹瀉可能就能猜出來誰喫的是真正的鎂片。
雖然補鎂可能會讓你覺得你睡得更好了(主觀感受改善),但如果你看硬指標,比如總睡眠時間(TST),鎂組和安慰劑組往往沒有統計學差異。
換句話說,你可能並沒有真的睡得更久,你只是在早上醒來時心情更好了一些。

更讓人頭疼的是安慰劑效應。在 Nielsen 2010 年的研究中,安慰劑組的 PSQI 評分從 10.4 降到了 6.6——這改善幅度大得驚人,以至於鎂組雖然改善得更多一點,但在統計學上根本拉不開差距。而在 Schuster 2025 年針對甘氨酸鎂的最新 RCT對照研究中,雖然主要終點勉強達到了顯著性(p=0.049,險勝),但在壓力、疲勞、情緒等所有次要終點上,鎂都沒有擊敗安慰劑。
還有一個問題是樣本量。Held 2002 年關於慢波睡眠的研究,樣本量只有 12 人。著名的 Abbasi 2012 年研究也只有 46 人。相比之下,正經的安眠藥物三期臨牀通常需要 300 到 1000 人。
如果你不是嚴重缺鎂,或者你還年輕力壯,補鎂往往就像給滿電的手機充電一樣徒勞無功。
比如 ZMA 的神話破滅。在生物黑客圈,ZMA(天冬氨酸鋅鎂)曾經被奉爲運動後的恢復神劑。然而,一項針對健身男性的 RCT 顯示,在部分睡眠剝奪的狀態下,ZMA 對睡眠潛伏期、睡眠效率或碎片化指數都沒有任何改善。結論很殘酷:如果你的飲食已經達標,額外補充 ZMA 對你的體能和睡眠沒有任何加成。
要小心哪些問題?
除了可能浪費錢,補鎂也有其他風險。
首先是補鎂的絕對禁區:腎功能損害。
腎臟是鎂排泄的唯一途徑。對於肌酐清除率低於 30 mL/min 的患者來說,補鎂極易導致高鎂血癥,進而引發低血壓、心律失常,甚至心臟驟停。
很多慢性腎病早期的人並不知道自己有腎功能問題,所以,在開始任何補鎂計劃之前,最好先確認你的腎臟是否準備好了。否則,你可能是在拿自己的心臟開玩笑。
二是“腹瀉”和“軟便”問題。這是最常見的副作用,也是最尷尬的。
在 Held 2002 年的研究中,爲了達到提升慢波睡眠的效果,研究人員使用了高劑量(約 729 毫克)的鎂。結果100% 的受試者(12 人中的 12 人)都出現了軟便。
很多鎂鹽本質上就是滲透性瀉藥。長期使用,你可能會發現自己對它們產生了依賴。
從腹瀉率來說,硫酸鎂> 氧化鎂 ≈氯化鎂 ≈ 檸檬酸鎂 > 甘氨酸鎂
另外,不同人對鎂的腸道耐受性差異極大。有的人300mg即腹瀉,也有人800mg無症狀。
三是吸收率的邊際遞減。
不要以爲喫多少就能補多少。鎂的吸收主要依靠腸壁上的專用蛋白來搬運,搬運工有限,一次喫太多會搬不過來。
研究顯示,鎂的吸收率與劑量成反比。當鎂的劑量從120 mg (相當於一頓富含鎂的飯或小劑量補劑)增加到 972 mg (相當於一次性吞下2-3倍的日推薦量,即“Mega-dosing”)時,吸收率就會從 65% 暴跌至 11%。
一次性猛補,基本上就是在製造昂貴的加鎂尿液和糞便。
最後,是藥物相互作用問題。
最好在喫鎂片之前,整理好你正在服用的藥物和補劑,去諮詢藥物方面的專家。
| 風險類別 | 具體情況/ 條件 | 應對策略 |
| 絕對禁忌 | 腎功能不全 / 腎衰竭 | 嚴禁自行補充。腎臟是排鎂的唯一途徑,腎功能受損會導致致命的高鎂血癥(心臟驟停)。 |
| 罕見/嚴重風險 | 高鎂血癥 | 症狀:低血壓、噁心、反射消失、呼吸抑制、昏迷。通常發生在腎衰患者或靜脈注射過量時。 |
| 絕對禁忌 | 重症肌無力 | 鎂會加重肌無力症狀。 |
| 絕對禁忌 | 心臟傳導阻滯 | 高鎂會進一步減慢心率和傳導。 |
| 藥物相互作用 | 雙磷酸鹽 (骨質疏鬆藥),不要同時服用 | 鎂會與藥物結合成不溶複合物,降低藥效。需間隔2小時以上。 |
| 藥物相互作用 | 四環素/喹諾酮類抗生素 | 同上,鎂會大幅降低抗生素吸收。需間隔2-4小時。 |
| 藥物相互作用 | 保鉀利尿劑 | 可能導致鎂瀦留,增加高鎂血癥風險。需醫生評估。 |
| 常見副作用 | 腹瀉 / 軟便 | 尤其是氧化鎂、檸檬酸鎂。分次服用或改用甘氨酸鎂可緩解。 |
| 常見副作用 | 胃腸道不適 / 噁心 | 隨餐服用可顯著減少噁心感。 |
回到最開始的問題。鎂片可以改善睡眠嗎?
視情況而定。
如果你是一個壓力巨大、飲食不夠均衡健康、年紀稍長、但腎功能沒有問題的失眠者,鎂可能會有幫助。
但如果你是一個飲食健康的年輕人,補鎂可能只是在製造昂貴的尿液。
保守派策略
適用人羣:飲食均衡、無明顯睡眠障礙、擔心副作用的人羣。
策略1: 飲食優化(天然鎂源)
通過均衡飲食(深綠色蔬菜、種子、堅果和全穀物)達到充足的鎂攝入(男性420mg、女性320mg),無需補充鎂劑。
可以多喫:南瓜子、腰果、菠菜、黑巧克力等。
策略2:非藥物的睡眠干預(證據強於鎂)
CBT-I (認知行爲療法)> 光療(晨間強光) > 限制睡眠時間(提升睡眠效率) > 冥想/正念 (降低皮質醇,改善主觀睡眠)

激進派策略
適用人羣:追求睡眠數據優化、處於高壓環境的人羣。
1️⃣檢查:腎功能、紅細胞鎂。
2️⃣鎂片選擇
| 鎂的形式 (Form) | 生物利用度(吸收率) | 腦部穿透力 | 典型用途 | 核心證據/特點 | 推薦指數 (針對睡眠) |
| L-蘇糖酸鎂 | 中-高 | 高 | 認知增強、改善記憶、助眠 | 唯一經動物實驗證實能顯著提升腦脊液鎂水平的形式。價格昂貴。 | ⭐⭐⭐⭐⭐ (適合高壓焦慮的腦力勞動者) |
| 甘氨酸鎂 | 高 | 中 | 睡眠、放鬆、抗焦慮 | 通過二肽通道吸收,腸胃耐受性極好 。甘氨酸本身也是抑制性神經遞質,有協同助眠作用。 | ⭐⭐⭐⭐⭐ (性價比首選,腸胃敏感者必選) |
| 乙酰牛磺酸鎂 | 高 | 中-高 | 抗焦慮、心臟健康 | 牛磺酸可與鎂協同抗焦慮。適合心悸/焦慮型失眠。 | ⭐⭐⭐⭐ (針對焦慮型) |
| 檸檬酸鎂 | 中-高 | 低 | 補鎂、便祕 | 吸收率優於氧化鎂 ,但高劑量有輕微瀉藥效應。性價比高,適合普通補充。 | ⭐⭐⭐ (預算有限者) |
| 氧化鎂 | 極低 (~4%) | 極低 | 抗酸劑、便祕 | 吸收率極差,大部分隨糞便排出。常導致腹瀉。但也有些研究用了它且有效。 | ⭐⭐ (不推薦,除非爲了通便 |
| 經皮鎂 (鎂油/鎂浴) | 低/無 | 無 | 局部肌肉放鬆? | 科學不支持。皮膚屏障極難穿透,血清鎂無顯著變化 。所謂“有效”多爲安慰劑或局部物理效應。 | 智商稅預警)。皮膚是用來當屏障的,不是用來喫飯的。 |
| 複方製劑 (Mg + 褪黑素/B6) | 混合 | 混合 | 強效助眠 | 效果通常最強,但往往是褪黑素在起作用。適合短期倒時差或嚴重失眠 | ⭐⭐⭐ (需警惕成分依賴) |
附錄:鎂相關論文
綜述與薈萃分析:
| 研究標題/作者/年份 | 研究類型 | 覆蓋範圍 | 核心結論 | |
| Veronese et al. 2020[1] | 傘形綜述 | 鎂與多種健康結果 | 強證據:鎂能減少偏頭痛頻率/強度、減少孕期住院。 中等證據:降低舒張壓 (~2 mmHg)。 觀察性證據:高攝入量與低糖尿病風險相關。 | 確認了鎂在神經系統(偏頭痛)和代謝(糖尿病)方面的益處,但對睡眠的結論較少,更多側重於慢性病預防。 |
| Mah & Pitre 2021[2] | 薈萃分析 | 老年失眠患者 (3項RCTs, N=151) | 入睡快了,但沒睡更久。 入睡潛伏期顯著縮短 (-17.36分鐘),但總睡眠時間(TST)無顯著增加。 | 鎂的侷限性:能幫你縮短入睡時間,但不能強行延長睡眠時間。 |
| Arab et al. 2023 [3] | 系統綜述 | 鎂與睡眠健康 (RCTs + 觀察性) | 矛盾的結果。觀察性研究顯示“喫鎂多的人睡得好”,但RCTs(干預實驗)結果不一致,無法得出確切結論。 | 再次印證了“飲食攝入”與“補劑干預”的差異。健康的生活方式(高鎂飲食)比單純吞藥片更有效。 |
| Pardo et al. 2021[4] | 系統綜述 | 生物利用度 (14項研究) | 有機 > 無機。有機鎂(檸檬酸、天冬氨酸等)生物利用度普遍優於無機鎂(氧化鎂)。吸收率隨劑量增加而降低。 | 確立了“少量多次”和“選擇有機鹽”的補充原則。 |
| Boyle et al. 2017[5] | 系統綜述 | 主觀焦慮與壓力 | 提示性益處。對輕度焦慮和經前綜合徵(PMS)有益,但證據質量較差。 | 鎂對焦慮的效果可能優於對睡眠的效果,特別是與B6聯用時。 |
| Chan & Lo 2022[6] | 系統綜述 | 膳食補劑與睡眠 | 鎂並非主角。氨基酸、褪黑素和維生素D對睡眠質量(PSQI)改善更顯著。鎂更多是作爲維生素D代謝的輔因子被提及。 | 不要只盯着鎂,它可能是維生素D發揮作用的“幕後推手”。 |
人體干預性研究:
| 研究 | 研究對象 (N) | 補劑形式 & 劑量 | 基線鎂狀態 | 協同成分 | 核心發現 | 副作用/不良反應 | 研究侷限性 |
| Abbasi et al. 2012[7] | 老年失眠患者 (60-75歲) (N=46), | 氧化鎂500 mg/天 (約 300mg 元素鎂) | 缺乏(<0.95 mmol/L) | 無 | 顯著改善:ISI失眠指數、入睡潛伏期、睡眠效率。客觀指標(腎素、褪黑素)升高,皮質醇降低。總睡眠時間(TST)無顯著差異。 | 無明顯副作用 | 樣本量小;僅針對老年缺鎂人羣,年輕人不可直接推導。 |
| Held et al. 2002[8] | 健康老年人 (N=12, 交叉試驗) | 泡騰片 元素鎂~729 mg/天 (屬於極高劑量,接近推薦攝入量的2倍) | 正常 | 無 | 客觀腦電圖(EEG)改善:慢波睡眠(SWS)顯著增加,皮質醇分泌減少。 | 100% 受試者出現軟便;1例水腫。 | 劑量極高(接近耐受上限)導致全員腸胃反應;樣本極小(N=12)。 |
| Schuster et al. 2025[9] | 睡眠差的健康成人 (N=155) | 甘氨酸鎂250 mg/天 | 未測 (回顧發現低攝入者效果好) | 甘氨酸 (1.5g) | 邊緣顯著:ISI指數改善 (p=0.049)。其他心理指標無差異。 | 極少 (安慰劑組副作用反而更多) | p值處於臨界點(0.049),統計學意義勉強;完全依賴主觀問卷,無客觀數據。 |
| Rondanelli et al. 2011[10] | 長期護理機構的老人 (N=43) | 鎂 225 mg/天 | 未知 | 褪黑素 (5 mg)鋅 (11.25 mg) | 效果驚人:PSQI評分大幅下降,生活質量顯著提高。 | 無明顯副作用 | 嚴重混雜:使用了5mg高劑量褪黑素(強效助眠),無法剝離鎂的單獨貢獻。 |
| Noah et al. 2021[11] | 壓力大且低鎂成人 (N=264) | 乳酸鎂300 mg/天 | 低 (0.66-0.84 mmol/L) | 維生素 B6 (30 mg) | 協同效應:對於嚴重壓力 亞組,"鎂+B6"比"單用鎂"改善壓力分數多24%。 | 腹瀉 (4.5%) | 事後分析(Post-hoc),證據力度弱於預設終點;無純安慰劑組對比。 |
| Nielsen et al. 2010[12] | 睡眠差的老年人 (>51歲) (N=100) | 檸檬酸鎂320 mg/天 | 混合 | 無 | 無效 (睡眠):PSQI改善顯著,但安慰劑組也改善了(強安慰劑效應)。僅在高CRP炎症亞組中看到抗炎效果。 | 無 | 經典的“安慰劑效應”案例;證明了鎂對非缺鎂人羣的睡眠可能無效。 |
| Gallagher et al. 2024[13] | 睡眠剝奪的健身男性 (N=16) | ZMA(天冬氨酸鎂鋅) 450 mg Mg + 30 mg Zn | 充足 (飲食達標) | 鋅, B6 | 無效:對睡眠結構、認知功能、運動表現均無改善。 | 無 | 天花板效應:受試者基線營養充足,補充劑淪爲“昂貴的尿液”。 |
| Gholizadeh-Moghaddam 2023[14] | PCOS (多囊) 女性 (N=64) | 氧化鎂250 mg/天 | 正常 (2.35 mg/dL) | 無 | 無效:對睡眠質量(PSQI)、高雄激素症狀均無顯著改善。 | 無 | 受試者基線不缺鎂;使用了吸收率較低的氧化鎂。 |
| Breus et al. 2024[15] | 非臨牀失眠成人 (N=31) | 納米氯化鎂 1g(元素鎂~120mg) | 未測 | 無 | 有效:主觀睡眠質量(PSQI)和客觀深睡時長(Oura Ring)改善。 | 無 | 利益衝突:由補劑廠商資助;樣本小;週期短(2周)。 |
| Supakatisant & Phupong 2015[16] | 孕婦 (腿抽筋) (N=80) | 甘氨酸鎂 300 mg/天 | 低 (孕期生理性下降) | 無 | 有效:顯著減少腿抽筋頻率和強度 (vs 安慰劑)。 | 噁心 (25.6%) 腹瀉 (14%) | 孕期特異性高,普通人蔘考價值有限;甘氨酸鎂也出現了較高的腸胃反應。 |
| Liu et al. 2016[17] | 認知障礙老人 (N=44) | L-蘇糖酸鎂 1.5-2 g (鹽重) | 未測 | 無 | 混合:認知功能顯著改善。但睡眠和焦慮改善被強安慰劑效應掩蓋,無統計學差異。 | 胃腸道不適 (20%) | 樣本小;主要終點是認知,睡眠是次要終點且未達標。 |
人體觀察性研究和隊列研究:
| 研究名稱/來源 | 研究對象 (樣本量N) | 比較方式 | 核心發現 | 研究侷限性 |
| Zhang et al. 2022 (CARDIA Study)[18] | 美國年輕成人 (N=3964) | 縱向追蹤 | 睡眠時長:高鎂攝入者短睡風險降低 (OR=0.64)。 睡眠質量:總體人羣改善處於邊緣顯著 (p=0.051);但在非抑鬱人羣中顯著有效。 | 抑鬱症狀是強幹擾因子;鎂攝入量是通過問卷估算的,存在回憶偏差。 |
| Alshammari et al. 2025[19] | 沙特大學生 (N=305) | 橫斷面 | 關聯顯著:低鎂攝入與短睡眠(<5h)和日間功能障礙顯著相關。 性別差異:女性睡眠質量普遍更差。 | 樣本同質化嚴重(全是學生);未測血鎂;橫斷面設計無法推導因果。 |
| Ikonte et al. 2019[20] | 美國成人 (NHANES) (N=26211) | 橫斷面 | 短睡者營養缺乏:睡眠<7小時的人羣,鈣、鎂、維D的攝入不足率顯著更高。 | 無法推斷因果。是缺鎂導致睡得少,還是睡得少導致喫得差所以缺鎂? |
| Grandner et al. 2014[21] | 美國成人 (NHANES) (N=4548) | 橫斷面 | 入睡困難:與低鎂攝入無顯著關聯(主要與硒、鈣、維D有關)。 日間嗜睡:與低鉀有關,鎂未顯示顯著性。 | 結果與其他研究矛盾;提示鎂可能不是單一決定因素,需考慮整體微量元素平衡。 |
| Cao et al. 2018[22] | 中國成人 (江蘇) (N=1487) | 縱向追蹤 (5年) | 性別差異:高鎂攝入顯著降低女性日間入睡風險 (OR=0.12),但在男性中無效。 打鼾:無關聯。 | 顯著的性別差異提示激素可能參與調節;中國飲食結構與西方不同,可能影響結果普適性。 |
| Luo et al. 2024[23] | 美國成人 (NHANES) (N=20,585) | 橫斷面 | OSA風險:高MDS評分者OSA風險增加3倍。 無效:與失眠、不寧腿綜合徵無顯著關聯。 | 使用了MDS評分而非直接測鎂,這是一種間接推算;未排除藥物干擾。 |
參考文獻
[1]Veronese, N., Demurtas, J., Pesolillo, G., Celotto, S., Barnini, T., Calusi, G., ... & Barbagallo, M. (2020). Magnesium and health outcomes: An umbrella review of systematic reviews and meta-analyses of observational and intervention studies. European journal of nutrition, 59(1), 263-272.
[2] Mah, J., & Pitre, T. (2021). Oral magnesium supplementation for insomnia in older adults: a systematic review & meta-analysis. BMC complementary medicine and therapies, 21(1), 125.
[3]Arab, A., Rafie, N., Amani, R., & Shirani, F. (2023). The role of magnesium in sleep health: a systematic review of available literature. Biological trace element research, 201(1), 121-128.
[4]Pardo, M. R., Vilar, E. G., Martín, I. S. M., & Martín, M. A. C. (2021). Bioavailability of magnesium food supplements: A systematic review. Nutrition, 89, 111294.
[5]Boyle, N. B., Lawton, C., & Dye, L. (2017). The effects of magnesium supplementation on subjective anxiety and stress—a systematic review. Nutrients, 9(5), 429.
[6]Chan, V., & Lo, K. (2022). Efficacy of dietary supplements on improving sleep quality: a systematic review and meta-analysis. Postgraduate medical journal, 98(1158), 285-293.
[7]Abbasi, B., Kimiagar, M., Sadeghniiat, K., Shirazi, M. M., Hedayati, M., & Rashidkhani, B. (2012). The effect of magnesium supplementation on primary insomnia in elderly: A double-blind placebo-controlled clinical trial. Journal of research in medical sciences: the official journal of Isfahan University of Medical Sciences, 17(12), 1161.
[8]Held, K., Antonijevic, I. A., Künzel, H., Uhr, M., Wetter, T. C., Golly, I. C., ... & Murck, H. (2002). Oral Mg2+ supplementation reverses age-related neuroendocrine and sleep EEG changes in humans. Pharmacopsychiatry, 35(04), 135-143.
[9]Schuster, J., Cycelskij, I., Lopresti, A., & Hahn, A. (2025). Magnesium bisglycinate supplementation in healthy adults reporting poor sleep: a randomized, placebo-controlled trial. Nature and science of sleep, 2027-2040.
[10]Rondanelli, M., Opizzi, A., Monteferrario, F., Antoniello, N., Manni, R., & Klersy, C. (2011). The effect of melatonin, magnesium, and zinc on primary insomnia in long‐term care facility residents in Italy: a double‐blind, placebo‐controlled clinical trial. Journal of the American Geriatrics Society, 59(1), 82-90.
[11]Noah, L., Dye, L., Bois De Fer, B., Mazur, A., Pickering, G., & Pouteau, E. (2021). Effect of magnesium and vitamin B6 supplementation on mental health and quality of life in stressed healthy adults: Post‐hoc analysis of a randomised controlled trial. Stress and Health, 37(5), 1000-1009.
[12]Nielsen, F. H., Johnson, L. K., & Zeng, H. (2010). Magnesium supplementation improves indicators of low magnesium status and inflammatory stress in adults older than 51 years with poor quality sleep. Magnesium Research, 23(4), 158-168.
[13]Gallagher, C., Austin, V., Dunlop, K. A., Dally, J., Taylor, K., Pullinger, S. A., & Edwards, B. J. (2024). Effects of supplementing zinc magnesium aspartate on sleep quality and submaximal weightlifting performance, following two consecutive nights of partial sleep deprivation. Nutrients, 16(2), 251.
[14]Gholizadeh‐Moghaddam, M., Ghasemi‐Tehrani, H., Askari, G., Jaripur, M., Clark, C. C., & Rouhani, M. H. (2023). Effect of magnesium supplementation in improving hyperandrogenism, hirsutism, and sleep quality in women with polycystic ovary syndrome: A randomized, placebo‐controlled clinical trial. Health science reports, 6(1), e1013.
[15]Breus, M. J., Hooper, S., Lynch, T., & Hausenblas, H. (2024). Effectiveness of magnesium supplementation on sleep quality and related health outcomes for adults with poor sleep quality: a randomized double-blind placebo-controlled crossover trial.
[16]Supakatisant, C., & Phupong, V. (2015). Oral magnesium for relief in pregnancy‐induced leg cramps: a randomised controlled trial. Maternal & child nutrition, 11(2), 139-145.
[17]Liu, G., Weinger, J. G., Lu, Z. L., Xue, F., & Sadeghpour, S. (2016). Efficacy and safety of MMFS-01, a synapse density enhancer, for treating cognitive impairment in older adults: a randomized, double-blind, placebo-controlled trial. Journal of Alzheimer’s disease, 49(4), 971-990.
[18]Zhang, Y., Chen, C., Lu, L., Knutson, K. L., Carnethon, M. R., Fly, A. D., ... & Kahe, K. (2022). Association of magnesium intake with sleep duration and sleep quality: findings from the CARDIA study. Sleep, 45(4), zsab276.
[19]Alshammari, A. A., Alsawad, K. A., Ahmed, N. K., Alsaadi, R., Alholieli, R. S., Alsaif, S., ... & Al-Hariri, M. (2025). Association Between Dietary Magnesium Intake and Sleep Quality in Saudi University Students: A Cross-Sectional Study. Nature and Science of Sleep, 3127-3136.
[20]Ikonte, C. J., Mun, J. G., Reider, C. A., Grant, R. W., & Mitmesser, S. H. (2019). Micronutrient inadequacy in short sleep: analysis of the NHANES 2005–2016. Nutrients, 11(10), 2335.
[21]Grandner, M. A., Jackson, N., Gerstner, J. R., & Knutson, K. L. (2014). Sleep symptoms associated with intake of specific dietary nutrients. Journal of sleep research, 23(1), 22-34.
[22]Cao, Y., Zhen, S., Taylor, A. W., Appleton, S., Atlantis, E., & Shi, Z. (2018). Magnesium intake and sleep disorder symptoms: findings from the Jiangsu Nutrition Study of Chinese adults at five-year follow-up. Nutrients, 10(10), 1354.
[23]Luo, X., Tang, M., Wei, X., & Peng, Y. (2024). Association between magnesium deficiency score and sleep quality in adults: a population-based cross-sectional study. Journal of Affective Disorders, 358, 105-112.
遊識猷
作者:遊識猷
本文來自果殼,未經授權不得轉載.
如有需要請聯繫[email protected]
點個“小愛心”吧